题目内容
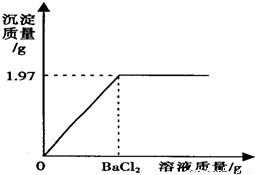
(2007?攀枝花)实验室里有一瓶固体烧碱因吸收了空气中的二氧化碳而部分变质.某化学兴 趣小组的同学为测定这瓶烧碱的纯度,称取该样品5g溶于水配成溶液,向其中逐滴加入氯化钡溶液至沉淀完全.反应过程中生成沉淀的质量与所用氯化钡溶液质量的关系如图所示,请计算该烧碱样品中:(1)碳酸钠的质量.
(2)氢氧化钠的质量分数.
【答案】分析:(1)根据碳酸钠与氯化钡反应的化学方程式和生成沉淀的质量,列出比例式,就可计算出样品中碳酸钠的质量;
(2)根据“ ×100%”,就可计算出样品中氢氧化钠的质量分数.
×100%”,就可计算出样品中氢氧化钠的质量分数.
解答:解:(1)设样品中碳酸钠的质量为x,
Na2CO3+BaCl2=BaCO3↓+2NaCl
106 197
x 1.97g
∴ ,
,
解之得:x=1.06g;
(2)氢氧化钠的质量分数= ×100%=78.8%.
×100%=78.8%.
答:(1)样品中碳酸钠的质量为1.06g;
(2)样品中氢氧化钠的质量分数为78.8%.
点评:本题主要考查学生运用化学方程式和质量分数公式综合分析和解决实际问题的能力.增加了学生分析问题的思维跨度,强调了学生整合知识的能力.
(2)根据“
 ×100%”,就可计算出样品中氢氧化钠的质量分数.
×100%”,就可计算出样品中氢氧化钠的质量分数.解答:解:(1)设样品中碳酸钠的质量为x,
Na2CO3+BaCl2=BaCO3↓+2NaCl
106 197
x 1.97g
∴
 ,
,解之得:x=1.06g;
(2)氢氧化钠的质量分数=
 ×100%=78.8%.
×100%=78.8%.答:(1)样品中碳酸钠的质量为1.06g;
(2)样品中氢氧化钠的质量分数为78.8%.
点评:本题主要考查学生运用化学方程式和质量分数公式综合分析和解决实际问题的能力.增加了学生分析问题的思维跨度,强调了学生整合知识的能力.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
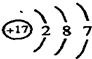 ,它在化学反应中一般易
,它在化学反应中一般易