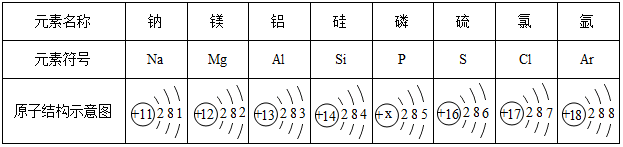
题目内容
5.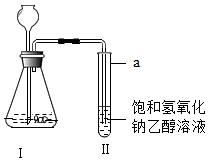 如图所示是某化学兴趣小组对二氧化碳与氢氧化钠溶液反应进行的创新实验.已知:20℃时,氢氧化钠在乙醇中的溶解度为17.3g,而碳酸钠在乙醇中几乎不溶解.请回答下列问题:
如图所示是某化学兴趣小组对二氧化碳与氢氧化钠溶液反应进行的创新实验.已知:20℃时,氢氧化钠在乙醇中的溶解度为17.3g,而碳酸钠在乙醇中几乎不溶解.请回答下列问题:(1)装置Ⅰ中用稀盐酸和石灰石制取二氧化碳气体的化学方程式为CaCO3+2HCl=CaCl2+H2O+CO2↑;
(2)将二氧化碳气体通入饱和氢氧化钠乙醇溶液中,有沉淀出现,出现这一现象的原因是20℃时,氢氧化钠在乙醇中的溶解度为17.3g,而碳酸钠在乙醇中几乎不溶解(请用文字表述).
分析 (1)根据碳酸钙和盐酸反应生成氯化钙、水和二氧化碳进行分析;
(2)根据氢氧化钠、碳酸钠在乙醇中的溶解度进行分析.
解答 解:(1)碳酸钙和盐酸反应生成氯化钙、水和二氧化碳,化学方程式为:CaCO3+2HCl=CaCl2+H2O+CO2↑;
(2)20℃时,氢氧化钠在乙醇中的溶解度为17.3g,而碳酸钠在乙醇中几乎不溶解,所以将二氧化碳气体通入饱和氢氧化钠乙醇溶于中,马上又沉淀出现.
故答案为:(1)CaCO3+2HCl=CaCl2+H2O+CO2↑;
(2)20℃时,氢氧化钠在乙醇中的溶解度为17.3g,而碳酸钠在乙醇中几乎不溶解.
点评 本题主要考查常见气体的发生装置与收集装置的探究,发生装置依据反应物的状态和反应条件选择,收集装置依据气体的密度和溶解性选择.

练习册系列答案
 开心快乐假期作业暑假作业西安出版社系列答案
开心快乐假期作业暑假作业西安出版社系列答案 名题训练系列答案
名题训练系列答案
相关题目
7.下列变化中,属于化学变化的是( )
| A. | 石油分馏 | B. | 干冰升华 | C. | 汽油挥发 | D. | 光合作用 |
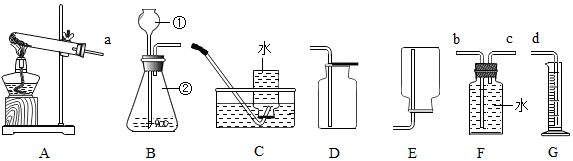
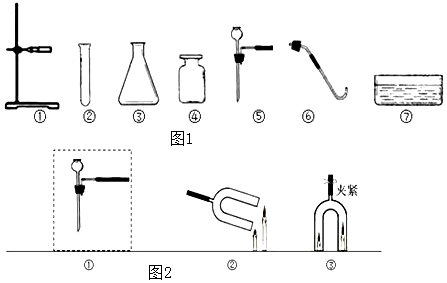
13.如图分别是有关实验室制取氧气的制备、干燥、收集和验满,下列说法正确的是( )

| A. | 装置①可作为氧气的发生装置,但不可用作二氧化碳的发生装置 | |
| B. | 装置②可用作氧气制取的收集装置 | |
| C. | 装置③可用作氧气制取的收集装置 | |
| D. | 装置④是收集氧气的验满方法 |
14.下列实验操作能达到实验目的是( )
| 实验目的 | 实验操作 | |
| A | 检验NaOH中含有Na2CO3 | 加入酚酞溶液、观察现象 |
| B | 鉴别氯化钠、硫酸铜和硝酸铵固体 | 取样、加水溶解、观察 |
| C | 除去CaCl2中混有少量HCl | 加入过量生石灰、过滤 |
| D | 除去KCl溶液中混有的MnO2 | 过滤、洗涤、干燥 |
| A. | A | B. | B | C. | C | D. | D |