题目内容
化学小组根据氨气还原氧化铜的反应,设计实验测定Cu元素的相对原子质量.已知:①2NH4Cl+Ca(OH)2=CaCl2+2NH3↑+2H2O ②氨气(NH3)是碱性气体
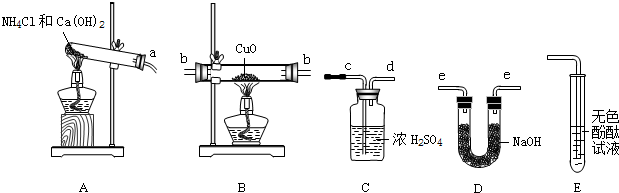
请结合下图回答问题.

(1)将纯净干燥的氨气通入B中,观察到玻璃管内黑色固体变为亮红色,管口有液滴,同时生成空气中含量最多的气体,写出B中发生反应的化学方程式为______ 3Cu+N2+3H2O
【答案】分析:(1)根据氨气还原氧化铜反应的现象,判断反应的生成物,其中空气中含量最多的气体是氮气,写出反应的化学方程式.
(2)Ⅰ.根据实验设想,在所提供的装置中选择简单、合理的装置组装能实现实验目的实验装置.
Ⅱ.分析所提供因素对实验结果的影响,判断其中会导致测定结果偏大的因素.
Ⅲ.根据对实验的理解,为达到测定目的,判断还可以采取的测量值.
解答:解:(1)将纯净干燥的氨气通入B中,观察到玻璃管内黑色固体变为亮红色,管口有液滴,同时生成空气中含量最多的气体;亮红色固体是铜,管口的液滴是水,空气中含量最多气体是氮气,反应的化学方程式为3CuO+2NH3 3Cu+N2+3H2O.
3Cu+N2+3H2O.
(2)Ⅰ.测定Cu元素相对原子质量的实验过程为:先称量CuO的质量,完全反应后测定生成水的质量,由此可知需测定生成水的质量,由于氨气(NH3)是碱性气体,不能用浓硫酸进行干燥;生成的氨气需先通过氢氧化钠干燥、再与氧化铜反应,最后用浓硫酸吸收生成的水,以测得生成水的质量.故装置连接合理的是ADBDC.
Ⅱ.设测定的氧化铜质量为A、生成水的质量为B,设铜的相对原子质量为m,
3CuO+2NH3 3Cu+N2+3H2O
3Cu+N2+3H2O
3m+48 54
A B
 m=
m=
①若Cu0未完全起反应,导致生成水的质量偏小,即B偏小,测定结果偏大;
②若CuO不干燥,加热过程水分蒸发,导致测得水的质量偏大,测定结果偏小;
③若Cu0中混有不反应的杂质,导致生成水的质量偏小,即B偏小,测定结果偏大;
④若NH4C1与Ca(OH)2混合物不干燥,但只要氨气干燥彻底,对氨气还原氧化铜的实验不产生影响.
故选项①③正确.
Ⅲ.根据反应的化学方程可发现,通过测定氧化铜与铜或铜与水等质量,也可计算出铜元素的相对原子质量.
故答案为:(1)3CuO+2NH3 3Cu+N2+3H2O;
3Cu+N2+3H2O;
(2)Ⅰ.③;Ⅱ.①③;Ⅲ.CuO和Cu.
点评:本题有一定难度,考查同学们新信息获取、处理及灵活运用所学知识进行解题的能力,从题干叙述的内容抽取有用的信息是正确解题的关键.
(2)Ⅰ.根据实验设想,在所提供的装置中选择简单、合理的装置组装能实现实验目的实验装置.
Ⅱ.分析所提供因素对实验结果的影响,判断其中会导致测定结果偏大的因素.
Ⅲ.根据对实验的理解,为达到测定目的,判断还可以采取的测量值.
解答:解:(1)将纯净干燥的氨气通入B中,观察到玻璃管内黑色固体变为亮红色,管口有液滴,同时生成空气中含量最多的气体;亮红色固体是铜,管口的液滴是水,空气中含量最多气体是氮气,反应的化学方程式为3CuO+2NH3
 3Cu+N2+3H2O.
3Cu+N2+3H2O.(2)Ⅰ.测定Cu元素相对原子质量的实验过程为:先称量CuO的质量,完全反应后测定生成水的质量,由此可知需测定生成水的质量,由于氨气(NH3)是碱性气体,不能用浓硫酸进行干燥;生成的氨气需先通过氢氧化钠干燥、再与氧化铜反应,最后用浓硫酸吸收生成的水,以测得生成水的质量.故装置连接合理的是ADBDC.
Ⅱ.设测定的氧化铜质量为A、生成水的质量为B,设铜的相对原子质量为m,
3CuO+2NH3
 3Cu+N2+3H2O
3Cu+N2+3H2O3m+48 54
A B
 m=
m=
①若Cu0未完全起反应,导致生成水的质量偏小,即B偏小,测定结果偏大;
②若CuO不干燥,加热过程水分蒸发,导致测得水的质量偏大,测定结果偏小;
③若Cu0中混有不反应的杂质,导致生成水的质量偏小,即B偏小,测定结果偏大;
④若NH4C1与Ca(OH)2混合物不干燥,但只要氨气干燥彻底,对氨气还原氧化铜的实验不产生影响.
故选项①③正确.
Ⅲ.根据反应的化学方程可发现,通过测定氧化铜与铜或铜与水等质量,也可计算出铜元素的相对原子质量.
故答案为:(1)3CuO+2NH3
 3Cu+N2+3H2O;
3Cu+N2+3H2O;(2)Ⅰ.③;Ⅱ.①③;Ⅲ.CuO和Cu.
点评:本题有一定难度,考查同学们新信息获取、处理及灵活运用所学知识进行解题的能力,从题干叙述的内容抽取有用的信息是正确解题的关键.

练习册系列答案
相关题目