题目内容
20.非金属单质具有类似金属与盐溶液之间的置换反应规律,即活动性较强的非金属可把活动性较弱的非金属从其盐溶液中置换出来,如在溶液中可发生下列反应:C12+2NaBr=2NaCl+Br2; Br2+2KI=2KBr+I2; I2+Na2S=2NaI+S↓(1)C12、Br2、I2中非金属活动性最强的Cl2>Br2>I2>S.
(2)判断下列化学方程式书写正确的有B.
A.C12+2NaI=2NaCl+I2 B.I2+2KBr=2KI+Br2C. C12+K2S=2KCl+S↓
分析 根据活动性较强的非金属可把活动性较弱的非金属从其盐溶液中置换出来,来比较非金属单质活动性的强弱,并据此判断反应的正误.
解答 解:(1)根据活动性较强的非金属可把活动性较弱的非金属从其溶液中置换出来,由反应Cl2+2NaBr=2NaCl+Br2可判断Cl2的活动性比Br2强;由Br2+2KI=2KBr+I2可判断Br2的活动性比I2强;由I2+Na2S=2NaI+S↓可判断I2的活动性比S强,综合以上判断,可得四种非金属单质Cl2、I2、Br2、S活动性的强弱关系为:Cl2>Br2>I2>S;
(2)A.由于Cl2的非金属活动性大于I2,Cl2+2NaI=2NaCl+I2 方程式书写正确;
B、由于Br2的活动性比I2强,该反应不能发生,方程式书写错误;
C、由于Cl2的非金属活动性大于S,C12+K2S═2KCl+S↓,方程式书写正确.
故答为:(1)Cl2>Br2>I2>S;(2)B.
点评 本题主要考查了对金属活动性顺序的应用.根据金属活动性顺序来判断反应的发生,或根据反应的发生剧烈程度判断金属的活动性强弱,从而加强学生对金属活动性顺序的理解.

练习册系列答案
相关题目
8.一氧化氮在常温下是一种难溶于水的气体,密度比空气略大;它能跟空气里的氧气迅速反应,生成二氧化氮.现要收集一氧化氮气体,可采用的方法是( )
| A. | 向上排空气法 | B. | 排水法或向下排空气法 | ||
| C. | 排水法或向上排空气法 | D. | 排水法 |
9.芯片是电脑、“智能”加点的核心部件,它是用高纯度硅制成的.下面是生产单质硅过程中的一个重要反应:SiO2+2C$\frac{\underline{\;高温\;}}{\;}$Si+2CO↑,该反应的基本类型是( )
| A. | 化合反应 | B. | 分解反应 | C. | 置换反应 | D. | 复分解反应 |
10.下列物质中,不属于碱的是( )
| A. | 纯碱 | B. | 氢氧化镁 | C. | 熟石灰 | D. | 烧碱 |

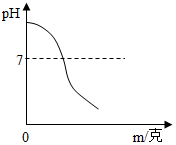 如图所示是稀硫酸与50克质量分数为5%的氢氧化钠溶液反应时,溶液的pH随加入溶液的质量m的变化关系图.请回答下列问题:
如图所示是稀硫酸与50克质量分数为5%的氢氧化钠溶液反应时,溶液的pH随加入溶液的质量m的变化关系图.请回答下列问题: (1)2008年05月08日10:39 新华社电,北京奥运圣火珠峰传递登山队成功登顶珠峰.这是第五棒、也是最后一棒火炬手次仁旺姆(左)在珠峰顶峰展示手中的“祥云”火炬(电
(1)2008年05月08日10:39 新华社电,北京奥运圣火珠峰传递登山队成功登顶珠峰.这是第五棒、也是最后一棒火炬手次仁旺姆(左)在珠峰顶峰展示手中的“祥云”火炬(电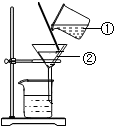 如图为精制粗盐时过滤装置的示意图,请回答:
如图为精制粗盐时过滤装置的示意图,请回答: