题目内容
2.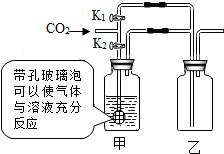 利用如图装置验证二氧化碳的部分性质,进行如下实验(甲、乙试剂瓶的体积均为250mL).
利用如图装置验证二氧化碳的部分性质,进行如下实验(甲、乙试剂瓶的体积均为250mL).实验一:若乙中盛有用紫色石蕊溶液染成的干燥的纸花,关闭K1,打开K2,通入潮湿的CO2气体,紫色纸花不变色,则甲中所盛试剂可能是浓硫酸或浓氢氧化钠溶液.关闭K2,打开K1,通入潮湿的CO2气体,紫色纸花变红,用化学方程式解释纸花变红的原因CO2+H2O═H2CO3.
实验二:若甲中盛有100mLNaOH溶液,乙中盛有100mLCa(OH)2溶液.验证二氧化碳与氢氧化钠发生了反应.
资料:通常状况下,1体积的水约能溶解1体积二氧化碳.
①甲中发生反应的化学方程式为CO2+2NaOH═Na2CO3+H2O.
②你设计的实验方案是关闭K1,打开K2,往导管中缓缓通入大于250mL的二氧化碳,若乙容器中无浑浊,则说明二氧化碳和氢氧化钠发生了反应.
分析 二氧化碳的化学性质有:既不能燃烧也不能支持燃烧,也不供给呼吸;能与水反应生成碳酸;能使澄清的石灰水变浑浊.若乙中盛有用紫色石蕊溶液染成的干燥的纸花,关闭K1,打开K2,通入潮湿的CO2气体,紫色纸花不变色,则甲中所盛试剂可能是:浓硫酸或浓氢氧化钠溶液;关闭K2,打开K1,通入潮湿的CO2气体,紫色纸花变红,用化学方程式解释纸花变红的原因:CO2+H2O═H2CO3;二氧化碳与氢氧化钠反应生成碳酸钠和水,配平即可;设计的实验方案是:关闭K1,打开K2,往导管中缓缓通入大于250mL的二氧化碳,若乙容器中无浑浊,则说明二氧化碳和氢氧化钠发生了反应.
解答 解:实验一:若乙中盛有用紫色石蕊溶液染成的干燥的纸花,关闭K1,打开K2,通入潮湿的CO2气体,紫色纸花不变色,则甲中所盛试剂可能是:浓硫酸或浓氢氧化钠溶液;关闭K2,打开K1,通入潮湿的CO2气体,紫色纸花变红,用化学方程式解释纸花变红的原因:CO2+H2O═H2CO3;碳酸能使紫色石蕊试液变红色,故答案为:浓硫酸或浓氢氧化钠溶液;CO2+H2O═H2CO3
实验二:二氧化碳与氢氧化钠反应生成碳酸钠和水,配平即可;设计的实验方案是:关闭K1,打开K2,往导管中缓缓通入大于250mL的二氧化碳,若乙容器中无浑浊,则说明二氧化碳和氢氧化钠发生了反应;故答案为:CO2+2NaOH═Na2CO3+H2O;关闭K1,打开K2,往导管中缓缓通入大于250mL的二氧化碳,若乙容器中无浑浊,则说明二氧化碳和氢氧化钠发生了反应.
点评 本考点考查了二氧化碳的性质和用途,二氧化碳与人类生活密切相关,在自然界中实现了碳循环.也充分体现了性质决定用途,用途又反映性质的理念.本考点基础性强,主要出现在填空题和实验题中.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
12.以下物质因为具有良好的吸水性,常用作气体的干燥剂,其中吸水过程中一定发生了化学变化的是( )
| A. | 浓硫酸 | B. | 生石灰 | C. | 烧碱固体 | D. | 氯化钙固体 |
13.下列变化属于化学变化的是( )
| A. | 湿衣服晾干 | B. | 冰雪融化 | C. | 香水挥发 | D. | 菜刀生锈 |
11.根据图所示实验,回答问题.
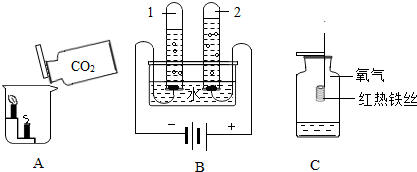
(1)实验A中的现象说明二氧化碳具有的性质是二氧化碳不支持燃烧也不能燃烧,且密度比空气大.
(2)实验B中反应的化学方程式为2H2O$\frac{\underline{\;通电\;}}{\;}$2H2↑+O2↑,该实验证明水由氢元素和氧元素组成.
(3)实验C中观察到的实验现象是剧烈燃烧,放热,火星四射,生成黑色固体.

(1)实验A中的现象说明二氧化碳具有的性质是二氧化碳不支持燃烧也不能燃烧,且密度比空气大.
(2)实验B中反应的化学方程式为2H2O$\frac{\underline{\;通电\;}}{\;}$2H2↑+O2↑,该实验证明水由氢元素和氧元素组成.
(3)实验C中观察到的实验现象是剧烈燃烧,放热,火星四射,生成黑色固体.
| 实验装置 | 实验操作 | 实验现象 |
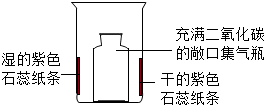 | ①在烧杯内壁上贴上干的和用水润湿的紫色石蕊纸条 ②将充满二氧化碳的敞口集气瓶轻轻放入烧杯中 | 一段时间后,湿的紫色石蕊纸条变为红色 |
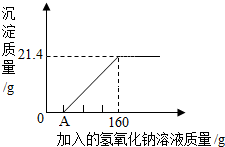 某化工厂的废水中只含有稀盐酸和氯化铁,小敏采集了该废水样品95.4g,并向其中滴加20%的氢氧化钠溶液至恰好完全反应,测得所加入的氢氧化钠溶液质量与反应生成的沉淀质量关系如图所示,已知上述反应后所得溶液在常温下为不饱和溶液,求该溶液中溶质的质量分数.
某化工厂的废水中只含有稀盐酸和氯化铁,小敏采集了该废水样品95.4g,并向其中滴加20%的氢氧化钠溶液至恰好完全反应,测得所加入的氢氧化钠溶液质量与反应生成的沉淀质量关系如图所示,已知上述反应后所得溶液在常温下为不饱和溶液,求该溶液中溶质的质量分数.