题目内容
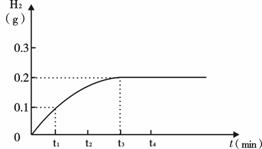
将Cu-Zn合金样品20g放入足量稀硫酸中,所产生氢气的质量与反应时间的关系如下图所示。试计算:
(1)原样品中所含锌的质量。
(2)实验测得20g该样品与154.7g某稀硫酸恰好完全反应,求此时所得溶
液中溶质的质量分数。
 |
解:设原样品中锌的质量为x,生成ZnSO4的质量为y,则:
Zn+H2SO4 =ZnSO4 + H2↑ ………………………………………………1分
65 161 2
x y 0.2g ………………………………………………1分
![]() x=6.5g …………………………………………………1分
x=6.5g …………………………………………………1分
![]() y=16.1g ………………………………………………1分
y=16.1g ………………………………………………1分
反应后溶液的质量为:154.7g+6.5g-0.2g=161g………………………………1分
溶液中溶质的质量分数为:![]() ×100%=10%………………………………1分
×100%=10%………………………………1分
答:原样品中锌的质量为6.5g,反应后溶液中溶质的质量分数为10%。

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目

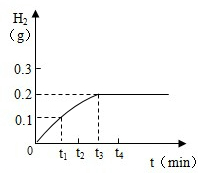 (2012?岳阳)将Cu-Zn合金样品20g放入足量稀硫酸中,所产生氢气的质量与反应时间的关系如图所示.试计算:
(2012?岳阳)将Cu-Zn合金样品20g放入足量稀硫酸中,所产生氢气的质量与反应时间的关系如图所示.试计算: