题目内容
19.冀东水泥厂是我国规模较大的水泥厂,该厂的化验室为了测定某矿山石灰石中碳酸钙的质量分数,取石灰石样品放在烧杯中,滴加适量稀盐酸至恰好完全反应(假设石灰石样品中杂质不与稀盐酸反应也不溶于水),最后测得生成气体的质量为4.4克,其他有关实验数据如下表:| 反应前 | 反应后 | |||
| 实验数据 | 烧杯的质量 | 石灰石样品的质量 | 盐酸的质量 | 烧杯和其中混合物的质量 |
| 61.4g | 12.5g | 未知 | 142.5g | |
分析 碳酸钙与稀盐酸反应生成氯化钙、水和二氧化碳,由生成二氧化碳气体的质量,由反应的化学方程式列式计算出参加反应的碳酸钙的质量,进而计算出石灰石中碳酸钙的质量分数即可.
解答 解:设参加反应的碳酸钙的质量为x
CaCO3+2HCl=CaCl2+H2O+CO2↑
100 44
x 4.4g
$\frac{100}{44}=\frac{x}{4.4g}$ x=10g
该石灰石中碳酸钙的质量分数为$\frac{10g}{12.5g}×$100%=80%.
答:该石灰石中碳酸钙的质量分数为80%.
点评 本题难度不大,掌握根据化学方程式的计算即可正确解答本题,解题时要注意解题的规范性.

练习册系列答案
相关题目
9.下列说法不正确的是( )
| A. | 蛋白质、糖类、脂肪都为机体活动提供能量 | |
| B. | 亚硝酸钠(NaNO2)被误作食盐食用,会导致中毒事故发生 | |
| C. | 为了防止大脖子病,可食用加入碘单质的食盐 | |
| D. | 点燃氢气前需要验纯 |
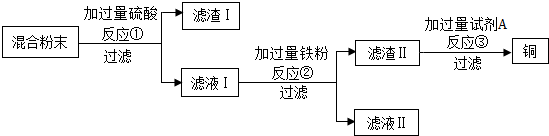
14. 某白色固体A可能含有碳酸钠、硫酸钠、氯化钠、硝酸钡中的一种或几种,进行如下实验:(信息提示:硫酸钠、硝酸钡溶液呈中性)
某白色固体A可能含有碳酸钠、硫酸钠、氯化钠、硝酸钡中的一种或几种,进行如下实验:(信息提示:硫酸钠、硝酸钡溶液呈中性)
①操作I是过滤.
②在沉淀B中加入足量稀硝酸,沉淀部分溶解.根据上述实验分析,A中一定含有的物质是Na2CO3、Na2SO4、Ba(NO3)2.写出沉淀部分溶解的化学方程式BaCO3+2HNO3=Ba(NO3)2+H2O+CO2↑.
③取少量滤液C于试管中,滴入酚酞,溶液变红,则C中一定含有的溶质是NaNO3、Na2CO3.
④为进一步确定固体A中可能存在的物质,对滤液C进行实验,完成下表.
 某白色固体A可能含有碳酸钠、硫酸钠、氯化钠、硝酸钡中的一种或几种,进行如下实验:(信息提示:硫酸钠、硝酸钡溶液呈中性)
某白色固体A可能含有碳酸钠、硫酸钠、氯化钠、硝酸钡中的一种或几种,进行如下实验:(信息提示:硫酸钠、硝酸钡溶液呈中性)①操作I是过滤.
②在沉淀B中加入足量稀硝酸,沉淀部分溶解.根据上述实验分析,A中一定含有的物质是Na2CO3、Na2SO4、Ba(NO3)2.写出沉淀部分溶解的化学方程式BaCO3+2HNO3=Ba(NO3)2+H2O+CO2↑.
③取少量滤液C于试管中,滴入酚酞,溶液变红,则C中一定含有的溶质是NaNO3、Na2CO3.
④为进一步确定固体A中可能存在的物质,对滤液C进行实验,完成下表.
| 实验操作 | 现象 | 结论 |
| 取滤液C少量,滴入足量Ba(NO3)2溶液;过滤后往滤液中滴入AgNO3溶液 | 产生白色沉淀 | 确定A固体中还含有氯化钠 |
16.现有一定质量的甲烷不完全燃烧,生成一氧化碳、二氧化碳和水蒸气的混合气体75g,经测定混合气体中碳元素的质量分数为16%,则参加反应的氧气的质量是( )
| A. | 48 g | B. | 56 g | C. | 59 g | D. | 64 g |
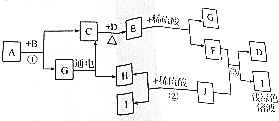 A一J是初中化学常见物质,A、G由相间的元素组成,常温下均为无色液体.B、E为黑色固体,D、J为金属单质,I为浅绿色溶液,这些物质的相互转化关系如图所示.
A一J是初中化学常见物质,A、G由相间的元素组成,常温下均为无色液体.B、E为黑色固体,D、J为金属单质,I为浅绿色溶液,这些物质的相互转化关系如图所示. 能源与环境问题是全球关注的热点问题,能源的开发与合理利用越来越重要.
能源与环境问题是全球关注的热点问题,能源的开发与合理利用越来越重要.