题目内容
10.食盐是维持人体正常生理活动必不可少的物质.低钠盐能预防高血压,碘盐能补充人体所需碘元素,工业上盐使用不当易使人中毒.(1)氯化钠中质量分数较大的是氯(填名称)元素.
(2)硫酸镁可以改变钠盐的“口味”,硫酸镁的化学式为MgSO4.
(3)碘盐中加了碘酸钾(KIO3),则KIO3中碘元素的化合价为+5价.
(4)工业用盐含NaNO2,NaNO2的名称为C(填序号).
A.磷酸钠 B.硝酸钠 C.亚硝酸钠.
分析 (1)根据化合物中各元素的相对原子量及质量分数分析;
(2)根据化合物化学式的书写一般规律:金属在前,非金属在后;氧化物中氧在后,原子个数不能漏,正负化合价代数和为零进行分析;
(3)根据在化合物中正负化合价代数和为零进行分析;
(4)根据NaNO2的名称为亚硝酸钠进行分析.
解答 解:(1)在NaCl中,钠元素的相对原子量为23,氯元素的相对原子量为35.5,故在氯化钠中氯元素的质量分数大;
(2)硫酸镁中镁元素显+2价,硫酸根显-2价,其化学式为MgSO4;
(3)根据在化合物中正负化合价代数和为零,钾元素的化合价为+1价,氧元素的化合价为-2价,设碘酸钾(KIO3)中碘元素的化合价为x价,则(+1)+x+(-2)×3=0,解得x=+5;
(4)NaNO2的名称为亚硝酸钠.
故答案为:(1)氯;(2)MgSO4;(3)+5价;(4)C.
点评 化学来源于生产、生活,也服务于生产、生活,与生产、生活实际相关的题目已渐渐成为化学考查的新宠.

练习册系列答案
相关题目
1.为了测定一瓶未密封保存的NaOH固体中NaOH的质量分数,小科采用沉淀法进行如下操作:①取15克样品于烧杯中,加足量水配成溶液;②在样品溶液中加入足量的BaCl2溶液;③待反应完全后,过滤.有关数据记录如表:
请回答下列问题:
(1)在反应前后的溶液中,下列元素质量保持不变的是A
A.钠元素 B.碳元素 C.钡元素 D.氧元素
(2)反应共生成沉淀19.7克
(3)原样品中NaOH的质量分数是多少?
| 反应前 | 反应后 | |
| 烧杯和样品溶液总质量/g | 加入的氯化钡溶液质量/g | 过滤后烧杯和溶液总质量/g(滤液的损失忽略不计) |
| 95 | 65 | 140.3 |
(1)在反应前后的溶液中,下列元素质量保持不变的是A
A.钠元素 B.碳元素 C.钡元素 D.氧元素
(2)反应共生成沉淀19.7克
(3)原样品中NaOH的质量分数是多少?
18.餐桌上的饮品种类丰富,下列饮品中属于溶液的是( )
| A. | 酸奶 | B. | 玉米糊 | C. | 冰水 | D. | 可乐 |
5.氯化钠由什么粒子构成?四位同学分别给出以下答案,你认为正确的是( )
| A. | 离子 | B. | 分子 | C. | 原子 | D. | 中子 |
15.下列反应属于复分解反应的是( )
| A. | CO2+H2O═H2CO3 | B. | 2HCl+Ca(OH)2═CaCl2+2H2O | ||
| C. | 2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑ | D. | 2Na+2H2O═2NaOH+H2↑ |
2.下列有关说法错误的是( )
| A. | 水的三态变化说明分子间具有间隙 | |
| B. | 原子不显电性是因为原子中质子数与中子数相等 | |
| C. | 五个二氧化硫分子可表示为5SO2 | |
| D. | Al3+可表示一个铝离子带三个单位的正电荷 |
9.某同学用一定量 Cu(NO3)2和 Zn(NO3)2的混合溶液进行了如图实验.则对溶液甲和固体乙成分的描述正确的是( )
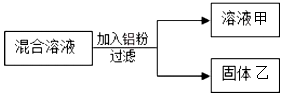

| A. | 溶液甲中一定有 Zn(NO3)2和 Al(NO3)3 | |
| B. | 溶液甲中一定有 Cu(NO3)2和 Al(NO3)3 | |
| C. | 固体乙中一定有 Cu,可能有 Zn和 Al | |
| D. | 固体乙中一定有 Cu和 Zn,可能有 Al |