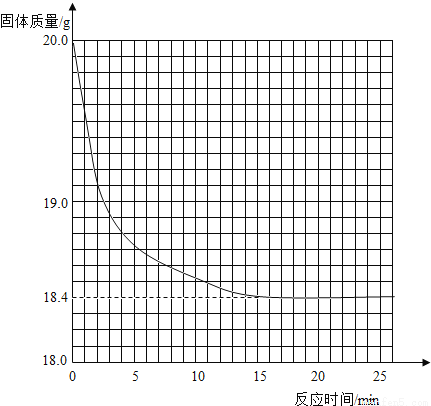
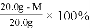题目内容
精还原铁粉是一种重要的化工原料,某兴趣小组对其进行下列研究:
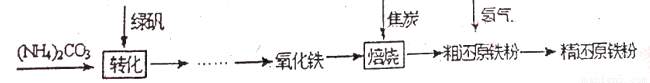
(物质制备)利用绿矾制备精还原铁粉的工艺流程如下:
粗还原铁粉中还含有少量铁的氧化物和Fe3C杂质,可用氢气在高温下进一步还原,其反应方程式为:
Fe3C+2H2 3Fe+CH4 FexOy+yH2
3Fe+CH4 FexOy+yH2 xFe+yH2O
xFe+yH2O
(1)已知焙烧中发生的主要反应是CO夺取氧化铁中的氧元素,得到单质铁与另一种碳的氧化物,请写出该反应的化学方程式_____________。
(2)焙烧中加焦炭的作用除了可以作燃料提供反应所需高温外,还能________。
(含量测定)甲同学为得到精还原铁粉并测定粗还原铁粉中氧和碳元素的质量分数,按如下装置进行实验。已知:3CH4+4Fe2O3 3CO2+6H2O+8Fe,浓硫酸有吸水性,可以吸收混合气体中的水热气,碱石灰不仅 能吸收水而且能吸收CO2。(假设每步反应都完全且不考虑装置内原有空气对测定结果的影响)。
3CO2+6H2O+8Fe,浓硫酸有吸水性,可以吸收混合气体中的水热气,碱石灰不仅 能吸收水而且能吸收CO2。(假设每步反应都完全且不考虑装置内原有空气对测定结果的影响)。
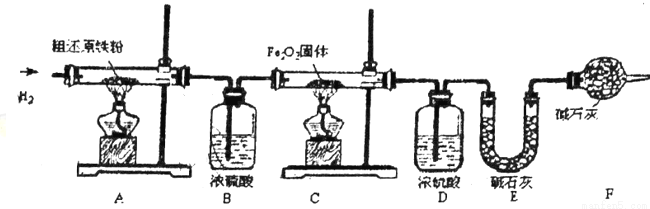
(3)主要实验步驟如下:
①按顺序组装仪器,检查装置的气密性,称量样品和必要装置的质量;
②缓缓通入纯净干燥的H2;③点燃C处酒精灯;④点燃A处酒精灯;⑤分别熄灭A、C处酒精灯;⑥再次缓缓通入H2;⑦再次称量必要装置的质量。
步骤②的目的是___________,步骤⑥的目的是__________。
(4)反应后C装置中的现象是_____________。
(5)若缺少装置F,则所测碳元素的质量分数将_____________(“偏大”、“偏小”或“不变”)。
 阅读快车系列答案
阅读快车系列答案如表是某同学错题本中整理的部分内容,其中不需要修改的是
A.化学用语 | B.仪器使用 |
氧化铝―AlO 2Ca2+―表示两个钙离子 | 直接在酒精灯火焰上加热的玻璃仪器―试管 胶头滴管取用试剂后―倒置或平放 |
C.物质的性质与用途 | D.物质鉴别 |
氦气密度小―填充探空气球 氮气常温下化学性质稳定―制氮肥、炸药 | 二氧化碳、氧气―加澄清石灰水 过氧化氢溶液、水―加二氧化锰 |
A. A B. B C. C D. D


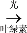 淀粉+O2 ,则生成的淀粉中一定含有____元素,可能含有_____元素。葡萄糖的化学是为 C6H12O6,每个分子是有______个原子构成,相对分子质量为_________(写出算式并计算),含碳元素的质量分数为________。
淀粉+O2 ,则生成的淀粉中一定含有____元素,可能含有_____元素。葡萄糖的化学是为 C6H12O6,每个分子是有______个原子构成,相对分子质量为_________(写出算式并计算),含碳元素的质量分数为________。