题目内容
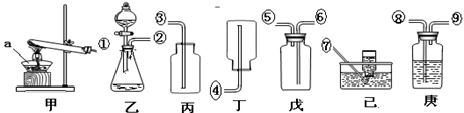
请结合下列实验装置完成问题.
(1)写出图中仪器a的名称:______.
(2)实验室制取二氧化碳的化学方程式是______,应选择的气体发生装置是______(填字母).
(3)实验室用氯酸钾与二氧化锰共热制取氧气的化学方程式是______△2KCl+3O2↑
【答案】分析:(1)根据常用仪器分析解答;
(2)根据发生装置的选取方法选择发生装置;依据反应原理书写方程式;
(3)根据氯酸钾制取氧气的反应原理书写方程式,氧气的密度比水小,据此分析回答;
(4)根据实验室制取氨气的反应物和反应条件选择发生装置;并依据氨气的性质选择合适的收集装置.
解答:解:(1)图中标号仪器是铁架台;
(2)实验室制取二氧化碳用大理石和稀盐酸常温反应制取,碳酸钙和盐酸反应生成氯化钙、水和二氧化碳,方程式是:2HCl+CaC03═CaCl2+H2O+CO2↑;反应物的状态是固态和液态,反应条件是常温,应选固-液不加热型的发生装置;
(3)氯酸钾以二氧化锰为催化剂加热生成氯化钾和氧气,方程式是:2KClO3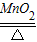 2KCl+3O2↑,若②通入,将水挤压到集气瓶底部并排尽,从而收集满氧气;
2KCl+3O2↑,若②通入,将水挤压到集气瓶底部并排尽,从而收集满氧气;
(4)实验室常用氯化铵固体与碱石灰固体共热来制取氨气,所以选择A发生装置;由于氨气密度比空气小,所以可用向下排空气法收集,由题意可知:氨气有刺激性气味,极易溶于水,为了防止其逸散到空气中污染空气,可以用水吸收,综上所述,可以选择H装置收集氨气,在出气管连接漏斗可增大氨气与水的接触面积,防止逸散到空气中,吸收的更彻底;
故答案为:
(1)铁架台;
(2)2HCl+CaC03═CaCl2+H2O+CO2↑;B;
(3)2KClO3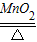 2KCl+3O2↑②;
2KCl+3O2↑②;
(4)A; H; 水能吸收氨气,防止逸散在空气中污染环境;.
点评:本题考查的是关于实验室制取气体的相关知识,注重了对学生知识的掌握、分析和解决问题能力的考查,要根据题意细心分析.
(2)根据发生装置的选取方法选择发生装置;依据反应原理书写方程式;
(3)根据氯酸钾制取氧气的反应原理书写方程式,氧气的密度比水小,据此分析回答;
(4)根据实验室制取氨气的反应物和反应条件选择发生装置;并依据氨气的性质选择合适的收集装置.
解答:解:(1)图中标号仪器是铁架台;
(2)实验室制取二氧化碳用大理石和稀盐酸常温反应制取,碳酸钙和盐酸反应生成氯化钙、水和二氧化碳,方程式是:2HCl+CaC03═CaCl2+H2O+CO2↑;反应物的状态是固态和液态,反应条件是常温,应选固-液不加热型的发生装置;
(3)氯酸钾以二氧化锰为催化剂加热生成氯化钾和氧气,方程式是:2KClO3
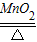 2KCl+3O2↑,若②通入,将水挤压到集气瓶底部并排尽,从而收集满氧气;
2KCl+3O2↑,若②通入,将水挤压到集气瓶底部并排尽,从而收集满氧气;(4)实验室常用氯化铵固体与碱石灰固体共热来制取氨气,所以选择A发生装置;由于氨气密度比空气小,所以可用向下排空气法收集,由题意可知:氨气有刺激性气味,极易溶于水,为了防止其逸散到空气中污染空气,可以用水吸收,综上所述,可以选择H装置收集氨气,在出气管连接漏斗可增大氨气与水的接触面积,防止逸散到空气中,吸收的更彻底;
故答案为:
(1)铁架台;
(2)2HCl+CaC03═CaCl2+H2O+CO2↑;B;
(3)2KClO3
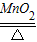 2KCl+3O2↑②;
2KCl+3O2↑②;(4)A; H; 水能吸收氨气,防止逸散在空气中污染环境;.
点评:本题考查的是关于实验室制取气体的相关知识,注重了对学生知识的掌握、分析和解决问题能力的考查,要根据题意细心分析.

练习册系列答案
 轻松课堂单元期中期末专题冲刺100分系列答案
轻松课堂单元期中期末专题冲刺100分系列答案
相关题目
通过学习,小明学会看多种实验室制取氧气的方法.结合下列装置图,按要求回答问题.
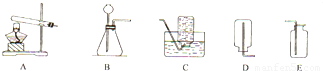
(1)实验室制取氧气常用方法有三种:一加热氯酸钾、二是分解过氧化氢溶液、三是 (用化学方程式表示)、
(2)小明参观某养鱼池时,好奇的发现农民向养鱼池中撒一种叫做过氧化钙的淡黄色固体,用来增加鱼池中的含氧量.小明刚学完氧气的实验室制法,于是他想到:
【提出问题】实验室能否用过氧化钙制取氧气?
【查阅资料】过氧化钙[CaO2]是一种淡黄色固体,无臭无味,易受潮,常温下化学性质稳定,在300℃时分解生成氧气,可用做鱼池增氧剂、杀菌剂等.
【猜想与论证】
猜想Ⅰ:实验室可以用加热过氧化钙的方法制取氧气.他的依据是 .
实验结论: .
猜想Ⅱ:实验室中可以用过氧化钙与水反应制取氧气.
实验结论: .
【分析与反思】虽然没有快速收集到大量氧气,但由此实验现象,小明认为农民用过氧化钙做增氧剂的主要原因是 .
【知识扩展】小明希望能找到加快过氧化钙与水反应的方法,请你帮他提成一条方便实验验证的建议: .

(1)实验室制取氧气常用方法有三种:一加热氯酸钾、二是分解过氧化氢溶液、三是 (用化学方程式表示)、
(2)小明参观某养鱼池时,好奇的发现农民向养鱼池中撒一种叫做过氧化钙的淡黄色固体,用来增加鱼池中的含氧量.小明刚学完氧气的实验室制法,于是他想到:
【提出问题】实验室能否用过氧化钙制取氧气?
【查阅资料】过氧化钙[CaO2]是一种淡黄色固体,无臭无味,易受潮,常温下化学性质稳定,在300℃时分解生成氧气,可用做鱼池增氧剂、杀菌剂等.
【猜想与论证】
猜想Ⅰ:实验室可以用加热过氧化钙的方法制取氧气.他的依据是 .
| 实验装置 | 实验主要 |
 | ①检查装置气密性:先将导管口伸入水面下,用受紧握试管,观察到 ,松开后,有少量水进入导管. ②将适量过氧化钙加入试管中,加入,导管口有大量气泡冒出. ③收集一瓶气体并检验气体. ④停止加热,熄灭酒精灯前,应 . |
猜想Ⅱ:实验室中可以用过氧化钙与水反应制取氧气.
| 实验装置 | 实验主要过程 |
| 该实验的发生装置应选择 ,收集装置可选择 或 .(填序号) | ①检验装置气密性. ②将水加入过氧化钙中,有少量细小气泡缓慢放出,该装置放置到第二天,集气瓶中只收集到极少量气体,震荡发生装置仍有少量细小气泡缓慢放出. |
【分析与反思】虽然没有快速收集到大量氧气,但由此实验现象,小明认为农民用过氧化钙做增氧剂的主要原因是 .
【知识扩展】小明希望能找到加快过氧化钙与水反应的方法,请你帮他提成一条方便实验验证的建议: .