题目内容
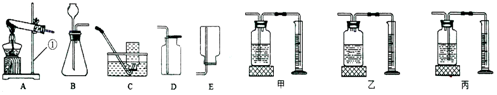
3.如图是初中化学实验室制取气体的一些装置图.根据要求回答问题.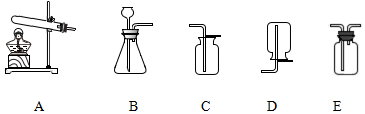
(1)实验室制取气体若选用A装置,除因为反应条件需要加热外,还因为反应物是固体.写一个用A装置制取某气体的化学方程式2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑,该气体可用C装置收集,检验是否收集满的方法是将带火星的木条平放在集气瓶口,木条复燃,证明该气体已收集满.
(2)气体X的密度比空气小,且不与酸反应,可由一种固体物质与水反应生成.要得到一瓶干燥的该气体,所选装置的连接顺序是AC(填字母),可选用浓硫酸做干燥剂.气体X在空气中燃烧的化学方程式为:
2X+5O2 $\frac{\underline{\;点燃\;}}{\;}$ 4CO2+2H2O,则X的化学式是C2H2.
分析 制取装置包括加热和不需加热两种,如果用双氧水和二氧化锰制氧气就不需要加热,如果用高锰酸钾或氯酸钾制氧气就需要加热.氧气的密度比空气的密度大,不易溶于水,因此能用向上排空气法和排水法收集.氧气的验满方法是:将带火星的木条平放在集气瓶口,木条复燃,证明氧气满了.气体X的密度比空气小,且不与酸反应,可由一种固体物质与水反应生成.要得到一瓶干燥的该气体,所选装置的连接顺序是AC,该气体不与酸反应,因此可以用浓硫酸干燥;根据质量守恒定律,等号两边各原子的种类和数目相等,在2X+5O2 $\frac{\underline{\;点燃\;}}{\;}$ 4CO2+2H2O中,则X是乙炔.
解答 解:(1)实验室制取气体若选用A装置,除因为反应条件需要加热外,还因为反应物是固体;如果用氯酸钾制氧气就需要加热,氯酸钾在二氧化锰做催化剂和加热的条件下生成氯化钾和氧气,配平即可;氧气的验满方法是:将带火星的木条平放在集气瓶口,木条复燃,证明氧气满了;故答案为:反应物是固体;2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑;将带火星的木条平放在集气瓶口,木条复燃;
(2)气体X的密度比空气小,且不与酸反应,可由一种固体物质与水反应生成.要得到一瓶干燥的该气体,所选装置的连接顺序是AC,该气体不与酸反应,因此可以用浓硫酸干燥;根据质量守恒定律,等号两边各原子的种类和数目相等,在2X+5O2 $\frac{\underline{\;点燃\;}}{\;}$ 4CO2+2H2O中,则X是乙炔;故答案为:AC;浓硫酸;C2H2;
点评 本考点主要考查了质量守恒定律、气体的制取装置和收集装置的选择,同时也考查了化学方程式的书写、气体的干燥和验满等,综合性比较强.气体的制取装置的选择与反应物的状态和反应的条件有关;气体的收集装置的选择与气体的密度和溶解性有关.本考点是中考的重要考点之一,主要出现在实验题中.


| A. | 属于非金属元素 | B. | 核内中子数为 60 | ||
| C. | 原子质量为 144.2 | D. | 核内质子数为 60 |
| A. | 水是由氢分子和氧分子构成的 | |
| B. | 试管a产生的气体是可使带火星的木条复燃 | |
| C. | 试管a,b中所产生的气体的质量比约为2:1 | |
| D. | 试管a,b所产生的气体的体积比约为2:1 |
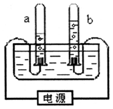
 如图所示是探究铁锈蚀条件的装置.调节L端与R端的液面高度一致,塞紧木塞,一周后观察.下列推断错误的是( )
如图所示是探究铁锈蚀条件的装置.调节L端与R端的液面高度一致,塞紧木塞,一周后观察.下列推断错误的是( )| A. | B管中铁钉不会锈蚀 | |
| B. | L端与R端液面高度左低右高 | |
| C. | 左右试管对比说明铁锈蚀与水、空气有关 | |
| D. | 若将A管中的水改为食盐水能加快铁的锈蚀 |
| A. | 生物体内的生理活动需要水的参与 | B. | 各种生物体内都含有大量的水 | ||
| C. | 有水的环境里才有生命 | D. | 水是生物呼吸作用的产物 |
| 操作步骤 | 实验结果 |
| (1)向废水中加入适量Cu后过滤 | 分离出滤液A和滤出物Ag |
| (2)向滤液A中加入Ba(OH)2溶液后过滤 | 滤出物是蓝色沉淀,滤液B中只含一种溶质 |
| (3)向滤液B中加入Na2CO3溶液后过滤 | 得到碳酸钡晶体 |
①你觉得此时他应如何填写滴加稀硝酸后的实验现象?B(填A:“沉淀全部溶解,产生气泡”或B:“沉淀部分溶解,产生气泡”填“序号”)
②事后,他在老师的帮助下进行了深入的分析,找到了出现这一问题的原因:由于前一组同学实验后用自来水洗涤试管,而自来水是含有氯离子,所以沉淀中含有AgCl (填化学式)不能被稀硝酸溶解.
 在做“铁在氧气里燃烧”实验时,小芳等同学进行了以下探究活动,请你一同参与.
在做“铁在氧气里燃烧”实验时,小芳等同学进行了以下探究活动,请你一同参与.(1)实验时要用砂纸擦去铁丝表面的铁锈,这个过程属于物理变化.
(2)明明同学实验时,集气瓶炸裂了,请你帮助他分析一下可能的原因集气瓶底没有放少量水或铺一层细沙.
(3)请用化学符号写出铁在氧气中燃烧反应的表达式:3Fe+2O2$\frac{\underline{\;点燃\;}}{\;}$Fe3O4,该反应属于化合(填“化合”或“分解”)反应.
(4)探究直径为0.38mm的铁丝燃烧是否需要纯氧
【实验内容】取0.38mm的铁丝,分别在体积分数为90%、70%、65%、60%、55%的氧气中进行实验,实验现象如下表所示:
| O2的体积分数 | 90% | 70% | 65% | 60% | 55% |
| 实验现象 | 燃烧剧烈、燃烧时间长,效果好 | 燃烧比90%弱,燃烧时间短,实验成功 | 燃烧比70%弱,燃烧时间比70%短,实验成功 | 燃烧比65%弱,燃烧时间更短,实验成功 | 难以燃烧,只是发红 |
【实验拓展】:(1)上述关于铁丝燃烧所需氧气最低浓度的结论是否合理,请说出理由?不合理 (填“合理”或“不合理”),理由:因为0.38mm的铁丝可能在氧气浓度为56%~59%的范围内燃烧.