题目内容
19.将溶质的质量分数为30%的硫酸溶液100克与溶质的质量分数为50%的硫酸溶液100克混合,混合溶液的溶质的质量分数为( )| A. | 80% | B. | 40% | C. | 15% | D. | 25% |
分析 根据同一溶质的浓溶液与稀溶液混合前后,溶质的质量之和不变,结合溶质质量=溶液质量×溶质的质量分数,进行分析解答.
解答 解:将溶质的质量分数为30%的硫酸溶液100克与溶质的质量分数为50%的硫酸溶液100克混合,同一溶质的浓溶液与稀溶液混合前后,溶质的质量之和不变,混合溶液的溶质的质量分数为$\frac{100g×30%+100g×50%}{100g+100g}$×100%=40%.
故选:B.
点评 本题难度不大,掌握同一溶质的浓溶液与稀溶液混合前后溶质的质量之和不变是正确解答本题的关键.

练习册系列答案
 名师伴你成长课时同步学练测系列答案
名师伴你成长课时同步学练测系列答案
相关题目
4.新型纳米材料MFe2Ox(3<x<4)中M表示+2价的金属元素,在反应中化合价不发生变化.常温下,MFe2Ox能使工业废气中的SO2转化为S,转化流程如下: ,已知MFeOy为+3价,下列说法中,不正确的是( )
,已知MFeOy为+3价,下列说法中,不正确的是( )
 ,已知MFeOy为+3价,下列说法中,不正确的是( )
,已知MFeOy为+3价,下列说法中,不正确的是( )| A. | SO2是大气污染物 | B. | SO2不是该反应的催化剂 | ||
| C. | y的数值为4 | D. | SO2发生了分解反应 |
9.某粗盐固体样品中含有少量CaCl2、MgCl2、Na2SO4、MgSO4和泥沙,进行以下操作可得到纯净的NaCl晶体:①加过量的NaOH溶液;②加H2O溶解;③加过量的BaCl2溶液;④过滤;⑤蒸发;⑥加过量的Na2CO3溶液;⑦加适量的稀盐酸,则正确的操作顺序是( )
| A. | ②①⑥③⑦④⑤ | B. | ②①③⑥④⑦⑤ | C. | ②⑥③①④⑦⑤ | D. | ①⑥②③④⑤⑦ |
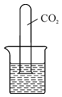 小明为了探究二氧化碳的性质,设计了如图所示的实验,在盛有水的烧杯中滴入紫色石蕊试液,将一个充满二氧化碳的试管倒立在其中.
小明为了探究二氧化碳的性质,设计了如图所示的实验,在盛有水的烧杯中滴入紫色石蕊试液,将一个充满二氧化碳的试管倒立在其中.