题目内容
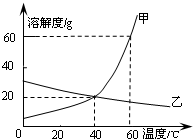 如图是甲、乙两种物质的溶解度曲线,下列叙述正确的是( )
如图是甲、乙两种物质的溶解度曲线,下列叙述正确的是( )| A、将60℃时,甲和乙的饱和溶液分别降温到40℃,所得溶液中甲和乙的质量分数不相等 |
| B、40℃时,甲的饱和溶液中溶质的质量分数是20% |
| C、采用降温的方法可以将乙的不饱和溶液转化为饱和溶液 |
| D、60℃时,在50g水中加入50g甲,充分溶解后溶液质量为100g |
考点:固体溶解度曲线及其作用,饱和溶液和不饱和溶液相互转变的方法,溶质的质量分数、溶解性和溶解度的关系
专题:溶液、浊液与溶解度
分析:A、根据甲、乙两物质的溶解度随温度变化的变化情况,可以判断降低温度时是否会析出晶体,进而确定溶质的质量分数的变化.
B、40℃时甲物质的溶解度是20g,溶质的质量分数为
×100%进行解答;
C、根据乙物质的溶解度随温度的升高而减小进行解答;
D、根据60℃时甲物质的溶解度是60g,则100g水中最多溶解60g,50g水中最多溶解30g,充分溶解后溶液质量为180g.
B、40℃时甲物质的溶解度是20g,溶质的质量分数为
| 20g |
| 100g+20g |
C、根据乙物质的溶解度随温度的升高而减小进行解答;
D、根据60℃时甲物质的溶解度是60g,则100g水中最多溶解60g,50g水中最多溶解30g,充分溶解后溶液质量为180g.
解答:解:
A、由于在60℃时,两种物质的溶解度大小关系是甲>乙,即在60℃时,两种物质的饱和溶液中溶质的质量分数甲>乙;由于甲的溶解度随温度的降低而减小,因此降温至40℃时,甲的溶液中都会有晶体析出,溶液都还是饱和溶液,由于在40℃时两种物质的溶解度甲=乙,而由于乙的溶解度随温度的降低而增大,因此降温至40℃时,它的饱和溶液就会变成不饱和溶液,但溶液中溶质的质量分数不变,由图可知,乙的溶液中溶质的质量分数还是比甲小.故对;
B、40℃时甲物质的溶解度是20g,溶质的质量分数为
×100%=16.7%,故错;
C、乙物质的溶解度随温度的升高而减小,升温的方法可以将乙的不饱和溶液转化为饱和溶液,故错;
D、根据60℃时甲物质的溶解度是60g,则100g水中最多溶解60g,50g水中最多溶解30g,充分溶解后溶液质量为180g,故错.
答案:A.
A、由于在60℃时,两种物质的溶解度大小关系是甲>乙,即在60℃时,两种物质的饱和溶液中溶质的质量分数甲>乙;由于甲的溶解度随温度的降低而减小,因此降温至40℃时,甲的溶液中都会有晶体析出,溶液都还是饱和溶液,由于在40℃时两种物质的溶解度甲=乙,而由于乙的溶解度随温度的降低而增大,因此降温至40℃时,它的饱和溶液就会变成不饱和溶液,但溶液中溶质的质量分数不变,由图可知,乙的溶液中溶质的质量分数还是比甲小.故对;
B、40℃时甲物质的溶解度是20g,溶质的质量分数为
| 20g |
| 100g+20g |
C、乙物质的溶解度随温度的升高而减小,升温的方法可以将乙的不饱和溶液转化为饱和溶液,故错;
D、根据60℃时甲物质的溶解度是60g,则100g水中最多溶解60g,50g水中最多溶解30g,充分溶解后溶液质量为180g,故错.
答案:A.
点评:主要考查了固体的溶解度曲线及固体的溶解度与温度间的关系,应加强对固体溶解度概念的理解,培养学生的理解能力.

练习册系列答案
相关题目
A、B、C、D、E是同一周期的五种主族元素,A和B的最高价氧化物对应的水化物显碱性,且碱性B>A;C和D两种元素对应的气态氢化物的稳定性C>D,E是这五种元素中原子半径最小的,则它们的原子序数由小到大的顺序为( )
| A、B<A<C<D<E |
| B、A<E<B<C<D |
| C、E<B<A<C<D |
| D、B<A<D<C<E |
下列实验现象描述正确的是( )
| A、硫在氧气中燃烧发出蓝紫色火焰,生成刺激性气味气体 |
| B、铁丝在氧气中燃烧火星四射,生成黑色的四氧化三铁 |
| C、木炭在氧气中燃烧发出白光,生成大量黑烟 |
| D、红磷在氧气中燃烧产生大量白色烟雾 |
过量的红磷在100mL的空气完全燃烧,冷却到室温后,剩余气体的体积约为( )
| A、80mL | B、60mL |
| C、40mL | D、20mL |
对于反应:X+Ca(OH)2=Y+Cu(OH)2↓,下列分析中正确的是( )
| A、该反应类型可能是置换反应 |
| B、Y 可能是CaCl2或Ca(NO3)2 |
| C、X和Y的相对分子质量之差为18 |
| D、X 可能是CuCl2或Fe2(SO4)3 |
有些化学变化可以用X+Y=M+R表示.关于此类变化,下列说法正确的是( )
| A、若X是单质,则该反应一定是置换反应 |
| B、若Y为金属,则该反应一定生成氢气 |
| C、若M和R为盐和水,该反应一定是中和反应 |
| D、若X为可溶性碱,Y为可溶性盐,则M和R可能是两种沉淀物 |
图表资料可以为我们提供很多信息,下列是某学生对图表资料的使用,其中正确的是( )
| A、根据元素周期表查某元素的原子序数或质子数 |
| B、根据原子的结构示意图可确定该原子的核内中子数 |
| C、根据酸碱盐的溶解性表,判断复分解反应能否进行 |
| D、根据相对原子质量表,判断某种元素原子的核外电子数目 |
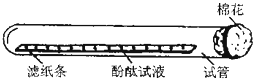 将滴有酚酞试液的滤纸条放在试管里,如图所示放在实验台上.
将滴有酚酞试液的滤纸条放在试管里,如图所示放在实验台上.