题目内容
4.我国第四套人民币中的一元硬币是钢芯镀镍(Ni),镍与稀硫酸能发生下列反应:Ni+H2SO4═NiSO4+H2↑.根据此材料及金属活动性顺序,请回答:
(1)铸造硬币用到的材料是金属材料(填“合成材料”或“金属材料”);
(2)写出Ni与CuSO4溶液发生置换反应的方程式:Ni+CuSO4═Cu+NiSO4.
分析 (1)依据硬币的组成成分分析材料的种类;
(2)根据金属活动性顺序的具体应用对金属的活动性进行分析,镍能置换出硫酸铜中的铜.
解答 解:(1)根据题干所知硬币的组成成分都是金属的合金,所以铸造以上硬币用到的材料都是金属材料;故填:金属材料;
(2)镍与稀硫酸能发生下列反应:Ni+H2SO4═NiSO4+H2↑. 说明镍在氢的前面,镍的化合价为+2价,故镍的活泼性比铜强,镍与硫酸铜反应生成铜和硫酸镍,反应的方程式为:Ni+CuSO4═Cu+NiSO4.
答案:(1)金属材料;(2)Ni+CuSO4═Cu+NiSO4.
点评 此题是一道与金属相关的考查题,解题的关键是充分理解和掌握金属活动性顺序表的意义以及其它相关的知识.

练习册系列答案
 备战中考寒假系列答案
备战中考寒假系列答案
相关题目
15.白酒中塑化剂(C16H22O4)的含量超标,会对人体造成损害,下列关于塑化剂的说法中,正确的是( )
| A. | 塑化剂由42个原子构成 | B. | 塑化剂由三种元素组成 | ||
| C. | 塑化剂的相对分子质量为278g | D. | 塑化剂属于氧化物 |
12.屠呦呦因发现对抗疟疾的青蒿素而获得.2015年的诺贝尔生理学或医学奖.青蒿素的化学式为C15H22O5,它在湿、热条件下易分解.下列说法正确的是( )
| A. | 提取青蒿素可以在高温下进行 | |
| B. | 青蒿素是由15个碳原子、22个氢原子、5个氧原予构成的 | |
| C. | 青蒿素中碳、氢、氧三种元素的原子个数比为15:22:5 | |
| D. | 青蒿素分子中含有碳、氢、氧三种元素 |
19. 小亮在实验室发现一瓶盛有无色溶液的试剂瓶.其标签破损.从残余部分只能看出溶质质量分数为10%.具体是什么物质无法辨认.老师告诉他,这瓶溶液可能是氢氧化钠、氯化钠、氢氧化钙或是碳酸钠溶液中的一种.
小亮在实验室发现一瓶盛有无色溶液的试剂瓶.其标签破损.从残余部分只能看出溶质质量分数为10%.具体是什么物质无法辨认.老师告诉他,这瓶溶液可能是氢氧化钠、氯化钠、氢氧化钙或是碳酸钠溶液中的一种.
【讨论交流】小亮查阅氢氧化钙常温下的溶解度为O.18g后,认为该溶液不可能是氢氧化钙,理由Ca(OH)2微溶于水,其溶液质量分数不可能为10%.
【实验验证】取少量样品于试管中,滴加无色酚酞试液,试液变红色,从而确定不可能是氯化钠溶液.
为了确定该溶液的成分,小亮又取少量样品于试管中,滴加氯化钙溶液,产生了白色沉淀,产生白色沉淀的反应的化学方程式是CaCl2+Na2CO3═CaCO3↓+2NaCl.小亮认为该溶液是碳酸钠溶液.
小红提出可能是氢氧化钠溶液变质了.于是他做了如下实验,请你参与:
【实验反思】
(1)小亮经过反思,向同学们提出如下建议,你认为合理的是①②③(填序号).
①要有严谨的科学实验的态度;②倾倒液体时应注意保护标签不被腐蚀;③试剂倾倒完毕应及时盖紧瓶塞;④无法辨认的药品,直接倒掉,无需保留试剂.
(2)小亮重新配置了10%的氢氧化钠溶液溶液,放入试剂瓶中,请你完成如图,给这个试剂瓶做一个标签.
 小亮在实验室发现一瓶盛有无色溶液的试剂瓶.其标签破损.从残余部分只能看出溶质质量分数为10%.具体是什么物质无法辨认.老师告诉他,这瓶溶液可能是氢氧化钠、氯化钠、氢氧化钙或是碳酸钠溶液中的一种.
小亮在实验室发现一瓶盛有无色溶液的试剂瓶.其标签破损.从残余部分只能看出溶质质量分数为10%.具体是什么物质无法辨认.老师告诉他,这瓶溶液可能是氢氧化钠、氯化钠、氢氧化钙或是碳酸钠溶液中的一种.【讨论交流】小亮查阅氢氧化钙常温下的溶解度为O.18g后,认为该溶液不可能是氢氧化钙,理由Ca(OH)2微溶于水,其溶液质量分数不可能为10%.
【实验验证】取少量样品于试管中,滴加无色酚酞试液,试液变红色,从而确定不可能是氯化钠溶液.
为了确定该溶液的成分,小亮又取少量样品于试管中,滴加氯化钙溶液,产生了白色沉淀,产生白色沉淀的反应的化学方程式是CaCl2+Na2CO3═CaCO3↓+2NaCl.小亮认为该溶液是碳酸钠溶液.
小红提出可能是氢氧化钠溶液变质了.于是他做了如下实验,请你参与:
| 实验步骤 | 实验现象 | 实验结论 |
| 取少量充分反应后的溶液于试管中,滴入无色酚酞试液 | 溶液变红色 | 该溶液是变质的氢氧化钠溶液. |
(1)小亮经过反思,向同学们提出如下建议,你认为合理的是①②③(填序号).
①要有严谨的科学实验的态度;②倾倒液体时应注意保护标签不被腐蚀;③试剂倾倒完毕应及时盖紧瓶塞;④无法辨认的药品,直接倒掉,无需保留试剂.
(2)小亮重新配置了10%的氢氧化钠溶液溶液,放入试剂瓶中,请你完成如图,给这个试剂瓶做一个标签.
16.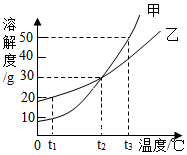 甲、乙两种不含结晶水的固体物质的溶解度曲线如图所示,下列说法中正确的是( )
甲、乙两种不含结晶水的固体物质的溶解度曲线如图所示,下列说法中正确的是( )
 甲、乙两种不含结晶水的固体物质的溶解度曲线如图所示,下列说法中正确的是( )
甲、乙两种不含结晶水的固体物质的溶解度曲线如图所示,下列说法中正确的是( )| A. | t1℃时,甲的溶解度大于乙的溶解度 | |
| B. | t3℃时,甲的饱和溶液溶质与溶液的质量比为1:2 | |
| C. | t2℃时,甲、乙溶液的溶质质量分数都为30% | |
| D. | t2℃时,质量相同的甲、乙饱和溶液分别升温至t3℃,为达到饱和状态,需加入甲的质量大于乙的质量 |
13.向盛有10mL的NaOH溶液(其中滴有少量无色酚酞溶液)的烧杯中逐滴加入稀盐酸用pH计(用来精确测定溶液pH的仪器)测定溶液的pH,所得数据如下:
(1)当加入稀盐酸的体积为10mL时,NaOH溶液和稀盐酸恰好完全反应.
(2)当加入稀盐酸的体积为3mL时,溶液显红色;当加入稀盐酸的体积为14mL时,溶液显无色.
(3)当烧杯中溶液的pH=2.1时,溶液中的溶质有:NaCl和HCl.
| 加入稀盐酸的体积/mL | 0 | 2 | 4 | 6 | 8 | 10 | 12 | 14 |
| 烧杯中溶液的pH | 12.9 | 12.7 | 12.5 | 12.3 | 11.9 | 7.0 | 2.1 | 1.9 |
(2)当加入稀盐酸的体积为3mL时,溶液显红色;当加入稀盐酸的体积为14mL时,溶液显无色.
(3)当烧杯中溶液的pH=2.1时,溶液中的溶质有:NaCl和HCl.
 目前,我们国家的能源主要依赖于化石燃料,它们属于不可再生资源.因此,开发利用新能源就显得格外重要.
目前,我们国家的能源主要依赖于化石燃料,它们属于不可再生资源.因此,开发利用新能源就显得格外重要. 化学与社会、人们的生活密切相关,请根据下列要求回答问题.
化学与社会、人们的生活密切相关,请根据下列要求回答问题.