题目内容
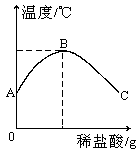
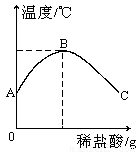
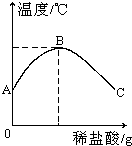 将稀盐酸慢慢滴入盛有氢氧化钠溶液的烧杯中,混合溶液的温度随加入稀盐酸质量的增加而变化,变化的情况如图所示.
将稀盐酸慢慢滴入盛有氢氧化钠溶液的烧杯中,混合溶液的温度随加入稀盐酸质量的增加而变化,变化的情况如图所示.(1)由图可知,该反应是
放热
放热
(填“放热”或“吸热”)反应.从A到B过程中,混合溶液的pH逐渐变小
变小
,B点表示的含义是盐酸和氢氧化钠恰好完全反应
盐酸和氢氧化钠恰好完全反应
,当混合溶液处于B、C点之间状态时,滴入酚酞试液变无
无
色.(2)该反应的基本类型是
复分解反应
复分解反应
.从微观角度看,反应的实质是H+
H+
和OH-
OH-
反应结合生成了水.分析:(1)根据图象可以看出随着盐酸的加入温度在逐渐上升,A到B的过程的反应实质是氢氧根离子逐渐减少,即氢氧化钠逐渐减少;B点对于温度是个转折点,对于反应进程也是个转折点,据此进行分析解答.
(2)根据反应物与生成物的种类、复分解反应的定义以及中和反应的微观过程分析.
(2)根据反应物与生成物的种类、复分解反应的定义以及中和反应的微观过程分析.
解答:解:(1)由图象可以看出,随着稀盐酸的加入,温度在逐渐的升高,说明稀盐酸与氢氧化钠溶液发生的反应是放热反应.从A到B过程中,氢氧化钠逐渐减少,碱性减弱,故pH值逐渐减小;在B点前后温度是两种情况,B点温度最高,B点表示酸碱恰好完全反应,反应后生成氯化钠和水,显中性,溶液中的pH=7.从B到C时盐酸过量,溶液呈酸性,酸溶液使酚酞不变色.
(2)盐酸与氢氧化钠反应生成氯化钠和水,反应物是两种化合物,交换成分后生成另外两种化合物,因此属于复分解反应.此过程中氢离子和氢氧根离子结合成水,而氯离子和钠离子反应前后不变,因此反应实质是氢离子和氢氧根离子结合成水.
故答案为:(1)放热 变小 盐酸和氢氧化钠恰好完全反应 无
(2)复分解反应(或中和反应) H+OH-
(2)盐酸与氢氧化钠反应生成氯化钠和水,反应物是两种化合物,交换成分后生成另外两种化合物,因此属于复分解反应.此过程中氢离子和氢氧根离子结合成水,而氯离子和钠离子反应前后不变,因此反应实质是氢离子和氢氧根离子结合成水.
故答案为:(1)放热 变小 盐酸和氢氧化钠恰好完全反应 无
(2)复分解反应(或中和反应) H+OH-
点评:本题难度不是很大,本题主要考查了结合图象考查了中和反应的应用,理解图象的含义、中和反应的实质是正确解答本题的关键.

练习册系列答案
 千里马走向假期期末仿真试卷寒假系列答案
千里马走向假期期末仿真试卷寒假系列答案
相关题目
某同学对盐酸溶液与氢氧化钠溶液的反应,按图所示过程进行探究:
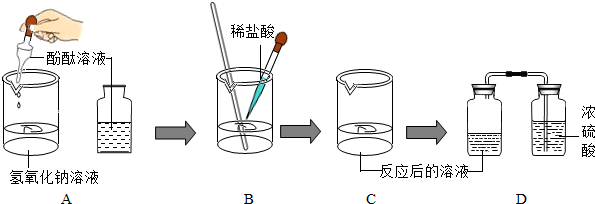
(1)填充实验过程空格项:
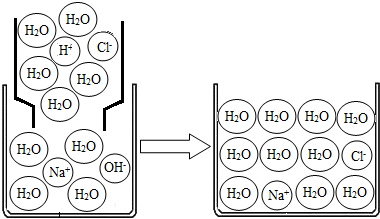
(2)模型探究:对上述过程采用微观模型加以认识,如图:
①氢氧化钠溶液与盐酸反应.反应中消失的离子有: .
②上图微观模型所反映的NaCl溶液溶质的质量分数: .

(1)填充实验过程空格项:
| 实验步骤 | 实验现象 | 实验结论 | |
| 步骤① | 取适量NaOH溶液放入烧杯中,滴入几滴酚酞试液. | ---------------------- | |
| 步骤② | 用胶头滴管将稀盐酸慢慢逐滴滴入到步骤①所得的溶液中,__________. | 溶液颜色逐渐变浅直到无色. | 氢氧化钠与稀盐酸反应. |
| 步骤③ | 当滴加稀盐酸至发生上述现象出现,立即停止. | -------------------- | ---------------------- |
| 步骤④ | 将③所得溶液移入广口瓶,并与盛有浓硫酸的广口瓶用导管连接导通,放置一段时间. | ______________. | ______________. |
①氢氧化钠溶液与盐酸反应.反应中消失的离子有:
②上图微观模型所反映的NaCl溶液溶质的质量分数:

(2008?房山区二模)某同学对盐酸溶液与氢氧化钠溶液的反应,按图所示过程进行探究:

(1)填充实验过程空格项:
(2)模型探究:对上述过程采用微观模型加以认识,如图:
①氢氧化钠溶液与盐酸反应.反应中消失的离子有:______.
②上图微观模型所反映的NaCl溶液溶质的质量分数:______.


(1)填充实验过程空格项:
| 实验步骤 | 实验现象 | 实验结论 | |
| 步骤① | 取适量NaOH溶液放入烧杯中,滴入几滴酚酞试液. | ---------------------- | |
| 步骤② | 用胶头滴管将稀盐酸慢慢逐滴滴入到步骤①所得的溶液中,__________. | 溶液颜色逐渐变浅直到无色. | 氢氧化钠与稀盐酸反应. |
| 步骤③ | 当滴加稀盐酸至发生上述现象出现,立即停止. | -------------------- | ---------------------- |
| 步骤④ | 将③所得溶液移入广口瓶,并与盛有浓硫酸的广口瓶用导管连接导通,放置一段时间. | ______________. | ______________. |
①氢氧化钠溶液与盐酸反应.反应中消失的离子有:______.
②上图微观模型所反映的NaCl溶液溶质的质量分数:______.