题目内容
15.小明同学为了测定市面销售的某品牌纯碱(杂质为氯化钠)中碳酸钠的质量分数,进行了如下实验:①在三个烧杯中分别加入11.0g样品及足量的水配成溶液;②向三个烧杯中分别加入一定质量的10.0%氯化钙溶液;③将充分反应后生成的沉淀过滤、洗涤、干燥,并称量得到的白色固体.实验所得数据见如表,请你分析并进行有关计算:样品中碳酸钠的质量分数是多少?(结果精确到0.1%)| 烧杯Ⅰ | 烧杯Ⅱ | 烧杯Ⅲ | |
| 加入10.0%氯化钙溶液的质量(g) | 55.5 | 120.0 | 150.0 |
| 白色固体的质量(g) | 5.0 | 10.0 | 10.0 |
分析 碳酸钠和氯化钙反应生成碳酸钙沉淀和氯化钠,根据沉淀碳酸钙质量可以计算碳酸钠质量,进一步可以计算样品中碳酸钠的质量分数.
解答 解:设碳酸钠质量为x,
由表中信息可知,反应生成碳酸钙质量是10.0g,
Na2CO3+CaCl2═CaCO3↓+2NaCl,
106 100
x 10.0g
$\frac{106}{x}$=$\frac{100}{10.0g}$,
x=10.6g,
样品中碳酸钠的质量分数为:$\frac{10.6g}{11.0g}$×100%=96.4%,
答:样品中碳酸钠的质量分数为96.4%.
点评 本题主要考查学生运用假设法和化学方程式进行计算和推断的能力,计算时要注意规范性和准确性.

练习册系列答案
相关题目
5.用化学符号表示:
(1)氧化镁中镁为+2价$\stackrel{+2}{Mg}$O;
(2)相对分子质量最小的氧化物H2O;
(3)发酵粉成分之一的小苏打NaHCO3;
(4)2个硫酸根离子2SO42-.
(1)氧化镁中镁为+2价$\stackrel{+2}{Mg}$O;
(2)相对分子质量最小的氧化物H2O;
(3)发酵粉成分之一的小苏打NaHCO3;
(4)2个硫酸根离子2SO42-.
3.某反应的微观示意图如图所示,下列说法错误的是( )
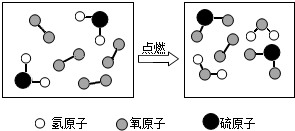

| A. | 反应物中有单质 | |
| B. | 生成物均是氧化物 | |
| C. | 反应前是混合物,反应后仍是混合物点燃 | |
| D. | 化学方程式是H2S+O2$\frac{\underline{\;点燃\;}}{\;}$SO2+H2O |
7.下列物质中,属于纯净物的是( )
| A. | 苹果醋 | B. | 矿泉水 | C. | 加碘的食盐 | D. | 氮气 |
4.化学与生活密切相关,下列食物中主要为人体提供维生素的是( )
| A. |  | B. |  | C. |  | D. |  |
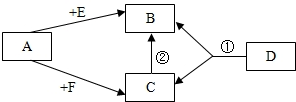 已知A、E、F是单质,B、C、D是化合物,它们分别是由碳、氢、氧三种元素中的一种或者几种组成.其中B是相对分子质量最小的氧化物,D物质很不稳定,容易分解生成B和C,它们之间的转化关系如图所示.
已知A、E、F是单质,B、C、D是化合物,它们分别是由碳、氢、氧三种元素中的一种或者几种组成.其中B是相对分子质量最小的氧化物,D物质很不稳定,容易分解生成B和C,它们之间的转化关系如图所示.