��Ŀ����
��10����37��.2009��12��14�գ����о����˳��п�ѧ֪ʶӦ����̽�����ܱ��������е�Ҷ����ǩ������Ŀ����ѡ���ڹ涨ʱ���ڣ������Լ��Ĵ�����ƣ���Ҷ������Ⱦɫ���滭���øƴ�ӵ������ӹ�������ʱij��ѡ��������200��10%������������Һ���������������Ƕ�ʣ����������Ʒ�Һ������������кʹ�����
��1������������Һʱ��Ҫ�������ƹ��� __ __ __ �ˣ�
��2����ȫ�кͷ�Һʱ��ȥ14.6%������100�ˣ���ʣ���Һ�к������������ʶ��ٿˣ�
�������Һ�е��������ʾ��������ᷢ����Ӧ��
��2���⣺��ʣ���Һ�к�������������x
NaOH+HCl=NaCl+H2O
40 36.5
x 100�ˡ�14.6%
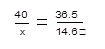 ������������������������1��
������������������������1��X=16�ˡ���������������������������������1��
�� ��������в�����λ���۷֣�
��ʣ���Һ�к�������������16�˽���:
��

��2011���㽭���ڣ�35�⣩ϸ�ĵ�ͬѧ�����ڼ�������ͭ����ʱ�����ŵ��̼�����ζ����������ͬѧ�ǵ���Ȥ���ѵ����ɵ�����ͭ��ĩ���Ⱥ��ֽܷ⣿�Ƿֽ�IJ�����ʲô�أ�
ͨ���������ϣ�ͬѧ���˽��
1������ͭ���ȷֽ���������ͭ�����塣��������SO2��SO3��O2�е�һ�ֻ��֡�����ʱ
�¶Ȳ�ͬ�����ɵ�����ɷ�Ҳ��ͬ��
2��SO2��SO3���ܱ���ʯ�����ա�
3��SO2��SO3���ܱ�����������Һ���ա�
��������롿���������غ㶨�ɲ²�����ijɷ֣�
I�� ֻ�� �� һ�֣� II������SO2��O2���֣� III������SO2��SO3��O2���֡�
�����ʵ�顿������ͼװ�ü�������ͭ��ĩֱ����ȫ�ֽ�
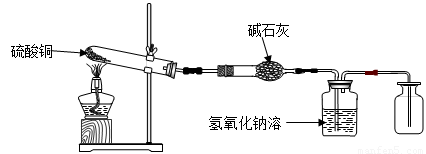
A B C D
����ȡ��ʵ��
��1���ô����ǵ�ľ�����뼯��ƿD������ľ���ܸ�ȼ��˵�������к��� �� ��
��2����֪����ͭ��ĩ����Ϊ10.0�ˣ���ȫ�ֽ��װ�õ������仯��ϵ���±���ʾ��
|
װ�� |
A���Թ�+��ĩ�� |
B |
C |
|
��Ӧǰ |
42.0�� |
75.0�� |
140.0�� |
|
��Ӧ�� |
37.0�� |
79.5�� |
140.0�� |
��ͨ�����㣬�ƶϳ���ʵ������������ͭ�ֽ�Ļ�ѧ����ʽ����һ�� �� ��
A.3CuSO4��3CuO+SO3��+2SO2��+O2 �� B. 4CuSO4��4CuO+2SO3��+2SO2��+O2��
C.5CuSO4��5CuO+SO3��+4SO2��+2O2 �� D. 6CuSO4��6CuO+4SO3��+2SO2��+O2��

