题目内容
1.某兴趣小组同学对实验室制备氧气的条件进行如下探究.【提出问题】①氧化铜是否也能做氯酸钾分解的催化剂?它是否比二氧化锰催化效果好?
【查阅资料】研究表明,许多金属氧化物对氯酸钾的分解有催化作用.分别用下列金属氧化物作催化剂,氯酸钾开始发生分解反应和反应剧烈时的温度如下表所示:
| 催化剂 温度/℃ 反应程度 | 氧化铁 | 氧化铝 | 氧化铜 | 氧化镁 |
| 开始反应 | 420 | 515 | 305 | 490 |
| 剧烈反应 | 490 | 540 | 350 | 545 |
设计并完成实验】Ⅰ.将3.0g氯酸钾放在试管中加热
Ⅱ.将3.0g氯酸钾与1.0g二氧化锰均匀混合加热
Ⅲ.将X g氯酸钾与1.0g氧化铜均匀混合加热
实验现象分析】Ⅲ中X的值应为3.0g,实验Ⅰ和Ⅲ比较可证明CuO改变KClO3分解的速率.将实验Ⅲ反应后的固体加水溶解、过滤、洗涤、干燥,若称量得到1.0g黑色粉末,再将黑色粉末和Xg氯酸钾混合加热,现象与实验Ⅲ相同,这些步骤是为了证明氧化铜在该化学反应前后质量和化学性质都不变.
【结论】氧化铜也能作氯酸钾分解的催化剂,实验Ⅲ中的化学反应的符号表达式为2KClO3$\frac{\underline{\;CuO\;}}{△}$2KCl+3O2↑.
【实验反思】实验Ⅱ和Ⅲ对比的目的是CuO对KClO3催化效果是否比MnO2好.
【提出问题】②MnO2的用量对 H2O2分解反应有何影响?
【设计并完成实验】利用图甲装置探究“MnO2的用量对 H2O2分解反应的影响”,实验中为3%H2O2溶液,装置中产生氧气的量可以用压强传感器测出(在等温条件下,产生氧气体积与装置内压强成正比,反应放热忽略不计.)
【讨论交流】(1)图乙是“0.1克MnO2与不同体积的3%H2O2溶液混合”的实验结果,从图中可以看出过氧化氢的用量越多,产生的氧气越多.

(2)当用“3%H2O2溶液8毫升与不同质量的MnO2混合”时,得到如图丙所示的曲线.曲线的斜率显示,当MnO2的用量增加到0.08克时,分解速度达到实验要求.在此实验条件下,若MnO2的质量有4克(一药匙),就能使如图C(填字母)烧杯中所装的3%H2O2溶液,其分解速度最接近实验要求.

分析 【查阅资料】比较表格中开始反应的温度和剧烈反应的温度,可以发现氧化铜的两个温度都比较低,方便操作.
【设计并完成实验】根据已有的知识进行分析,进行实验探究时要注意控制变量;根据控制双氧水的质量和质量分数相等才能比较出二氧化锰和氧化铜的催化效果分析.
【讨论交流】(1)根据图示可以看出H2O2的用量越多,产生的氧气越多;
(2)根据图中给出的比例分析.
解答 解:比较表格中开始反应的温度和剧烈反应的温度,可以发现氧化铜的两个温度都比较低.温度越低,加热反应时就越方便操作,所以氧化铜作催化剂最合适;
【设计并完成实验】
氯酸钾在二氧化锰的催化作用下加热能快速的产生氧气,进行实验探究时要注意控制变量,故X为3.0;Ⅰ与Ⅲ比较证明了氧化铜也可以加快氯酸钾的分解速率;根据催化剂的定义可以知道,要证明CuO能作为KClO3分解的催化剂,则还要证明在化学反应前后CuO的质量和化学性质都没有改变;实验Ⅲ中的化学反应为:2KClO3$\frac{\underline{\;CuO\;}}{△}$2KCl+3O2↑;Ⅱ与Ⅲ对比的目的是比较氧化铜与二氧化锰哪种物质对氯酸钾的催化作用更好;
【讨论交流】
(1)根据图示可以看出H2O2的用量越多,产生的氧气越多;
(2)由图示可知3%H2O2溶液8毫升与0.08克MnO2混合,分解速度达到实验要求,若MnO2的质量有4克需要3%H2O2溶液为$\frac{4g}{0.08g}$×8mL=400mL.
故答案为:
【查阅资料】氧化铜.
【实验现象分析】
3.0g,CuO改变KClO3分解的速率.
质量;化学性质.
【结论】2KClO3$\frac{\underline{\;CuO\;}}{△}$2KCl+3O2↑;
【实验反思】CuO对KClO3催化效果是否比MnO2好.
【讨论交流】
(1)过氧化氢的用量越多,产生的氧气越多.
(2)C.
点评 本题通过对比实验结果的分析,找到事物的内在联系,考查了学生分析问题的能力,同时也是对影响反应速率因素这一知识点的重点考查.

 应用题天天练四川大学出版社系列答案
应用题天天练四川大学出版社系列答案①过滤后液体仍然浑浊,原因可能是滤纸破损;
②氧气在氧化反应中提供氧,它具有氧化性;
③最外层电子为8的粒子一定是稀有气体原子;
④由一种元素组成的物质一定是单质;
⑤固体药品一般保存在细口瓶中;
⑥点燃蜡烛刚熄灭时产生的白烟,蜡烛重新燃烧,说明白烟有可燃性.
其中正确的是( )
| A. | ①②⑥ | B. | ①③⑥ | C. | ③④⑤ | D. | ①④⑥ |
| A. | Na2CO3 | B. | Al(NO3)3 | C. | Fe(NO3)3 | D. | Fe2(SO4)3 |
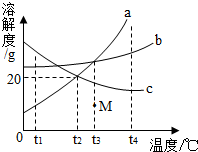 如图是a、b、c三种物质的溶解度曲线,请回答:
如图是a、b、c三种物质的溶解度曲线,请回答: