题目内容
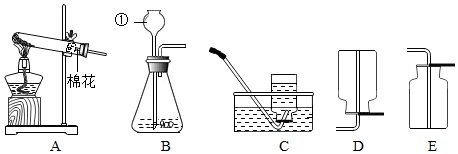
8.探究学习小组在实验室中用下图所示装置制取 CO2 并探究CO2 与过氧化钠(Na2O2)的反应.
查阅资料得知:过氧化钠(Na2O2)是一种淡黄色固体,能与CO2、H2O 发生反应:2Na2O2+2CO2═2Na2CO3+O2,2Na2O2+2H2O═4NaOH+O2↑.
请回答下列问题:
①装置A中发生反应的化学方程式为CaCO3+2HCl=CaCl2+H2O+CO2↑,利用装置A制取CO2的优点是能控制反应的发生与停止;
②装置 B 的作用是吸收二氧化碳中的氯化氢;
③装置D的作用是吸收CO2,此装置中发生的反应化学方程式为2NaOH+CO2=Na2CO3+H2O;
④装置E中收集到的气体是O2(填化学式),该气体还可以用下图装置中的ad进行收集(填写字母序号);

分析 ①根据碳酸钙和盐酸反应生成氯化钙、水和二氧化碳,A装置可以通过压强的改变实现固体和液体的分离进行分析;
②根据碳酸氢钠和盐酸反应生成氯化钠、水和二氧化碳进行分析;
③根据二氧化碳和氢氧化钠反应生成碳酸钠和水进行分析;
④根据过氧化钠和二氧化碳反应生成碳酸钠和氧气,氧气密度比空气大,不易溶于水进行分析.
解答 解:①碳酸钙和盐酸反应生成氯化钙、水和二氧化碳,化学方程式为:CaCO3+2HCl=CaCl2+H2O+CO2↑,A装置可以通过压强的改变实现固体和液体的分离,所以利用装置A制取CO2的优点是:能控制反应的发生与停止;
②碳酸氢钠和盐酸反应生成氯化钠、水和二氧化碳,所以装置B的作用是:吸收二氧化碳中的氯化氢;
③二氧化碳和氢氧化钠反应生成碳酸钠和水,化学方程式为:2NaOH+CO2=Na2CO3+H2O;
④过氧化钠和二氧化碳反应生成碳酸钠和氧气,氧气密度比空气大,不易溶于水,所以装置E中收集到的气体是O2,该气体还可以用下图装置中的ad进行收集.
故答案为:①CaCO3+2HCl=CaCl2+H2O+CO2↑,能控制反应的发生与停止;
②吸收二氧化碳中的氯化氢;
③2NaOH+CO2=Na2CO3+H2O;
④O2,ad.
点评 本题主要考查常见气体的发生装置与收集装置的探究,发生装置依据反应物的状态和反应条件选择,收集装置依据气体的密度和溶解性选择.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
19.青铜是合金,它是( )
| A. | 铜的氧化物 | B. | 铜单质 | C. | 铜的化合物 | D. | 铜的混合物 |
16.现有A、B、C三种金属,已知A能将C从它的溶液中置换出来,B能与盐酸或稀硫酸反应产生氢气,A不能与盐酸或稀硫酸反应.则这三种金属活动性由强到弱的顺序是( )
| A. | B>A>C | B. | B>C>A | C. | A>B>C | D. | 无法判断 |
13.发展绿色食品,避免“白色污染”,增强环保意识,是保护环境,提高人类生存质量的主要措施.通常的“白色污染”是指( )
| A. | 冶炼厂排放的白色烟尘 | B. | 石灰窑放出的白色粉尘 | ||
| C. | 聚乙烯等白色塑料垃圾 | D. | 白色建筑材料垃圾 |
20.类推是学习中常用的思维方法.现有一下类推结果,其中错误的是
①酸碱中和反应生成盐和水,所以生成盐和水的反应一定是中和反应;
②碱的水溶液显碱性,所以碱性溶液一定是碱溶液;
③氧化物都含有氧元素,所以含有氧元素的化合物一定是氧化物;
④复分解反应的反应物为两种化合物,生成物也是两种化合物,所以反应物为两种化合物,生成物也是两种化
合物的反应一定是复分解反应.( )
①酸碱中和反应生成盐和水,所以生成盐和水的反应一定是中和反应;
②碱的水溶液显碱性,所以碱性溶液一定是碱溶液;
③氧化物都含有氧元素,所以含有氧元素的化合物一定是氧化物;
④复分解反应的反应物为两种化合物,生成物也是两种化合物,所以反应物为两种化合物,生成物也是两种化
合物的反应一定是复分解反应.( )
| A. | 只有 ① | B. | 只有 ①②③ | C. | 只有②③④ | D. | ①②③④ |
18.下列物质中不作为空气污染物计入《环境空气质量标准》基本监测的是( )
| A. | 一氧化碳 | B. | 二氧化硫 | C. | 二氧化碳 | D. | PM10、PM2.5 |