题目内容
工业用苛化法制烧碱,其原理是以石灰石和纯碱为原料,经如图所示的一系列操作完成.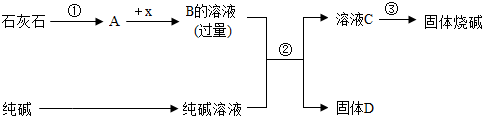
(1)①的反应条件是 ,X的化学式是 ;
(2)②的化学方程式是 ;
(3)溶液C的溶质是 (填化学式),③的方法是 ;
(4)判断该生产过程中可循环使用的一种物质及理由是 .

(1)①的反应条件是
(2)②的化学方程式是
(3)溶液C的溶质是
(4)判断该生产过程中可循环使用的一种物质及理由是
考点:物质的相互转化和制备,碳酸钙、生石灰、熟石灰之间的转化,盐的化学性质,书写化学方程式、文字表达式、电离方程式
专题:物质的制备
分析:根据石灰石的主要成分是碳酸钙,在高温下分解生成氧化钙和二氧化碳,氧化钙能与水反应生成氢氧化钙,氢氧化钙溶液与纯碱反应生成碳酸钙和氢氧化钠,据此结合题意进行分析解答.
解答:解:
(1)石灰石的主要成分是碳酸钙,在高温下分解生成氧化钙和二氧化碳,A为氧化钙,其化学式是CaO;X的化学式是H2O;
(2)反应②为氢氧化钙溶液与纯碱反应生成碳酸钙和氢氧化钠,反应的化学方程式为:Ca(OH)2+Na2CO3═CaCO3↓+2NaOH.
(3)反应②生成碳酸钙和氢氧化钠,故溶液C的溶质是NaOH,利用蒸发得到固体烧碱;
(4)判断该生产过程中可循环使用的一种物质及理由是碳酸钙;因为碳酸钙在高温下分解生成氧化钙和二氧化碳,氧化钙能与水反应生成氢氧化钙,而氢氧化钙溶液与纯碱反应生成碳酸钙和氢氧化钠.
故答案为:
(1)高温;H2O;
(2)Ca(OH)2+Na2CO3═CaCO3↓+2NaOH.
(3)NaOH,蒸发;
(4)碳酸钙;因为碳酸钙在高温下分解生成氧化钙和二氧化碳,氧化钙能与水反应生成氢氧化钙,而氢氧化钙溶液与纯碱反应生成碳酸钙和氢氧化钠.
(1)石灰石的主要成分是碳酸钙,在高温下分解生成氧化钙和二氧化碳,A为氧化钙,其化学式是CaO;X的化学式是H2O;
(2)反应②为氢氧化钙溶液与纯碱反应生成碳酸钙和氢氧化钠,反应的化学方程式为:Ca(OH)2+Na2CO3═CaCO3↓+2NaOH.
(3)反应②生成碳酸钙和氢氧化钠,故溶液C的溶质是NaOH,利用蒸发得到固体烧碱;
(4)判断该生产过程中可循环使用的一种物质及理由是碳酸钙;因为碳酸钙在高温下分解生成氧化钙和二氧化碳,氧化钙能与水反应生成氢氧化钙,而氢氧化钙溶液与纯碱反应生成碳酸钙和氢氧化钠.
故答案为:
(1)高温;H2O;
(2)Ca(OH)2+Na2CO3═CaCO3↓+2NaOH.
(3)NaOH,蒸发;
(4)碳酸钙;因为碳酸钙在高温下分解生成氧化钙和二氧化碳,氧化钙能与水反应生成氢氧化钙,而氢氧化钙溶液与纯碱反应生成碳酸钙和氢氧化钠.
点评:本题难度不大,掌握碳酸钙与氧化钙、氢氧化钙的相互转化、盐的化学性质是正确解答本题的关键.

练习册系列答案
相关题目
 表示
表示
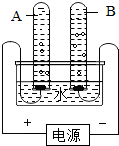 水是生命之源,爱护水资源是每个公民应尽的责任.请回答下列有关问题:
水是生命之源,爱护水资源是每个公民应尽的责任.请回答下列有关问题: 如图表示某物质在水(a)和酒精(b)中 的溶解度曲线.
如图表示某物质在水(a)和酒精(b)中 的溶解度曲线.