题目内容
石灰厂使用石灰石制取生石灰,反应的化学方程式为:CaCO3
CaO+CO2↑若生产含氧化钙25.2t的生石灰,则至少需要含碳酸钙90%的石灰石多少吨?
| ||
设用去的碳酸钙的质量为x,
CaCO3
CaO+CO2↑
100 56
x 25.2t
=
,
解得x=45t
则需要90%的石灰石的质量为
=50t,
答:需要含碳酸钙90%的石灰石质量为50t.
CaCO3
| ||
100 56
x 25.2t
| 100 |
| x |
| 56 |
| 25.2t |
解得x=45t
则需要90%的石灰石的质量为
| 45t |
| 90% |
答:需要含碳酸钙90%的石灰石质量为50t.

练习册系列答案
相关题目
 CaO+CO2↑若生产含氧化钙25.2t的生石灰,则至少需要含碳酸钙90%的石灰石多少吨?
CaO+CO2↑若生产含氧化钙25.2t的生石灰,则至少需要含碳酸钙90%的石灰石多少吨? CaO+CO2↑若生产含氧化钙25.2t的生石灰,则至少需要含碳酸钙90%的石灰石多少吨?
CaO+CO2↑若生产含氧化钙25.2t的生石灰,则至少需要含碳酸钙90%的石灰石多少吨? CaO+CO2↑若生产含氧化钙25.2t的生石灰,则至少需要含碳酸钙90%的石灰石多少吨?
CaO+CO2↑若生产含氧化钙25.2t的生石灰,则至少需要含碳酸钙90%的石灰石多少吨?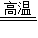 CaO+CO2↑若生产含氧化钙25.2t的生石灰,则至少需要含碳酸钙90%的石灰石多少吨?
CaO+CO2↑若生产含氧化钙25.2t的生石灰,则至少需要含碳酸钙90%的石灰石多少吨?