题目内容
2.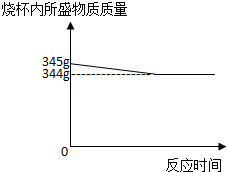 黄铜是常见的合金.为了测定某黄铜(成分为铜和锌)中锌的质量分数,某化学兴趣小组的同学进行了以下实验:取100g黄铜的样品,粉碎后加入装有245g足量稀硫酸的烧杯中,反应过程中测得烧杯内所盛物质的质量与相应时间记录如图:
黄铜是常见的合金.为了测定某黄铜(成分为铜和锌)中锌的质量分数,某化学兴趣小组的同学进行了以下实验:取100g黄铜的样品,粉碎后加入装有245g足量稀硫酸的烧杯中,反应过程中测得烧杯内所盛物质的质量与相应时间记录如图:请回答下列问题并计算:
(1)样品与稀硫酸反应生成的氢气的质量为1g.
(2)计算样品中锌的质量分数(写出具体计算过程,精确到0.1%)
分析 (1)锌能与稀硫酸反应生成氢气,而铜不能,故依据图象中反应前后物质的质量之差可求生成的氢气质量;
(2)依据氢气的质量利用化学方程式可求混合物中锌的质量,进而可求样品中锌的质量分数;
解答 解:(1)锌的金属活动性在氢前铜在氢后所以锌能与稀硫酸反应生成氢气,其质量为345g-344g=1g;故答案为:1;
(2)解:设100g样品中锌的质量为x,生成硫酸锌的质量为y
Zn+H2SO4=ZnSO4+H2↑
65 2
x 1g
$\frac{65}{x}=\frac{2}{1g}$
x=32.5g
样品中锌的质量分数为:$\frac{32.5g}{100g}$×100%=32.5%
答:样品中锌的质量分数为32.5%.
点评 利用质量守恒定律求出反应放出氢气的质量,是进行后面计算的基础,体现出运用知识分析问题的能力.

练习册系列答案
 智能训练练测考系列答案
智能训练练测考系列答案
相关题目
17. 液化石油气中含有丙烷,关于丙烷的下列叙述正确的是( )
液化石油气中含有丙烷,关于丙烷的下列叙述正确的是( )
 液化石油气中含有丙烷,关于丙烷的下列叙述正确的是( )
液化石油气中含有丙烷,关于丙烷的下列叙述正确的是( )| A. | 丙烷是由3个碳原子和8个氢原子构成的 | |
| B. | 丙烷中碳、氢元素的质量比为3:8 | |
| C. | 一个丙烷分子中有26个电子 | |
| D. | 丙烷属于无机化合物 |
15.下列说法正确的是( )
| A. | 混合物中元素的存在形态都是化合态 | |
| B. | 同种元素组成的不同单质互为同素异形体 | |
| C. | 金属与盐溶液发生置换反应后,溶液的质量一定增加 | |
| D. | 某物质能与碱反应生成盐和水,则该物质一定是酸 |
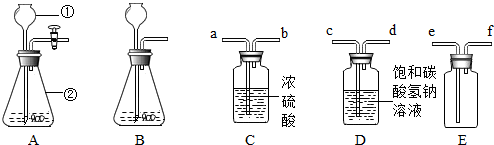

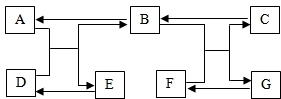 A~G是初中所学的常见物质,其转化关系如图所示(部分反应物和生成物、反应条件已略去),A、B常温下为无色气体且组成元素相同,实验室常用C制取B,变化A+D→B+E的现象是固体的颜色由黑变红.请回答下列问题:
A~G是初中所学的常见物质,其转化关系如图所示(部分反应物和生成物、反应条件已略去),A、B常温下为无色气体且组成元素相同,实验室常用C制取B,变化A+D→B+E的现象是固体的颜色由黑变红.请回答下列问题: