题目内容
6.如图①、②是氟元素、钙元素在元素周期表中的信息,A、B、C、D是四种粒子的结构示意图.
(1)氟元素的相对原子质量为19.00,钙元素的原子序数(即质子数)为20;
(2)D中的X=11;
(3)以上A、B、C、D粒子结构示意图中,表示稀有气体元素的原子的是A;表示离子的符号S2-
(4)B和C属于同种元素的粒子(用“A”、“C”、“D”填空).化学性质相似的粒子AC
(5)在A、B、C、D四种粒子中,两两结合形成的物质的化学式为Na2S氟元素、钙元素形成化合物的化学式CaF2.
分析 根据提供的信息可以判断相关方面的问题;
原子中,核电荷数=核内质子数=核外电子数=原子序数;
具有相同核电荷数的一类原子总称为元素;
最外层电子数相等的微观粒子的化学性质相似.
解答 解:(1)氟元素的相对原子质量是19.00,钙元素的原子序数(即质子数)为20.
故填:19.00;20.
(2)D中的X=2+8+1=11.
故填:11.
(3)以上A、B、C、D粒子结构示意图中,表示稀有气体元素的原子的是A,A是氦元素;
C表示硫离子,硫离子可以表示为S2-.
故填:A;S2-.
(4)B和C具有相同的核电荷数,属于同种元素的粒子;
化学性质相似的粒子是AC,这是因为AC的最外层电子数都是8个,化学性质不活泼.
故填:C;AC.
(5)在A、B、C、D四种粒子中,钠元素和硫元素组成硫化钠,可以表示为Na2S;
氟元素、钙元素形成的化合物是氟化钙,可以表示为CaF2.
故填:Na2S;CaF2.
点评 元素周期表反映了元素之间的内在联系,是学习化学的基础,要注意理解.

练习册系列答案
 口算题卡北京妇女儿童出版社系列答案
口算题卡北京妇女儿童出版社系列答案
相关题目
1.在实验中有时需要多次重复实验,其主要目的是为了( )
| A. | 避免偶然现象,使结果更真实 | B. | 得到较多的数据 | ||
| C. | 实验失败后重新再做 | D. | 得出不同的结论 |
11.分子和原子的本质区别是( )
| A. | 氧分子大,氧原子小 | |
| B. | 氧气既由氧分子构成,也由氧原子构成 | |
| C. | 氧气的化学性质由氧分子保持 | |
| D. | 在化学反应中,氧分子能再分,氧原子不能 |
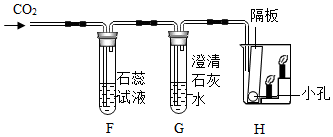 二氧化碳是一种温室气体.某化学兴趣小组利用如图所示装置对二氧化碳的性质进行验证:
二氧化碳是一种温室气体.某化学兴趣小组利用如图所示装置对二氧化碳的性质进行验证: 实验室可以利用稀盐酸等药品,通过连接如图装置制取二氧化碳、氢气.
实验室可以利用稀盐酸等药品,通过连接如图装置制取二氧化碳、氢气. 硝酸钾是初中化学常见的一种盐.请按要求填写下列有关空格:
硝酸钾是初中化学常见的一种盐.请按要求填写下列有关空格: 2013年3月26日晚,广药维C银翘片被央视曝光含毒,引起民众惊恐.维生素C是“维C银翘片”中的主要有效成分,它的化学式是C6H8O6.由此可知:
2013年3月26日晚,广药维C银翘片被央视曝光含毒,引起民众惊恐.维生素C是“维C银翘片”中的主要有效成分,它的化学式是C6H8O6.由此可知: