题目内容
20.如图是实验室常用的装置,请回答有关问题.
(1)写出仪器甲的名称锥形瓶.
(2)某小组在实验室选用B装置来制取二氧化碳气体,他们最好选择下列药品中的A、C(填序号).
A.大理石 B.纯碱 C.稀盐酸 D.稀硫酸
(3)实验前,将导管的胶皮管夹紧,向长颈漏斗中加水至浸没长颈漏斗下端管口,这样做的目的是检查装置的气密性.
(4)若用加热氯酸钾和二氧化锰混合物制取氧气,选用的发生装置是A,反应前后二氧化锰在固体混合物中质量分数将会变大(填“变大”、“变小”或“不变”).反应后,将剩余的固体经过滤、干燥得到二氧化锰固体,将二氧化锰加入到过氧化氢溶液中制备氧气,反应的化学方程式为2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑.
分析 锥形瓶是常用的反应容器,实验前,将导管的胶皮管夹紧,向长颈漏斗中加水至浸没长颈漏斗下端管口,这样做的目的是:检查装置的气密性;制取装置包括加热和不需加热两种,如果用双氧水和二氧化锰制氧气就不需要加热,如果用高锰酸钾或氯酸钾制氧气就需要加热.氧气的密度比空气的密度大,不易溶于水,因此能用向上排空气法和排水法收集.实验室制取CO2,是在常温下,用大理石或石灰石和稀盐酸制取的,碳酸钙和盐酸互相交换成分生成氯化钙和水和二氧化碳,因此不需要加热.二氧化碳能溶于水,密度比空气的密度大,因此只能用向上排空气法收集.
解答 解:(1)锥形瓶是常用的反应容器,故答案为:锥形瓶;
(2)实验室制取CO2,是在常温下,用大理石或石灰石和稀盐酸制取的,碳酸钙和盐酸互相交换成分生成氯化钙和水和二氧化碳,因此不需要加热;故答案为:A、C;
(3)实验前,将导管的胶皮管夹紧,向长颈漏斗中加水至浸没长颈漏斗下端管口,这样做的目的是:检查装置的气密性;故答案为:检查装置的气密性;
(4)如果用氯酸钾和二氧化锰制氧气就需要加热,反应前后二氧化锰在固体混合物中质量分数将会变大,因为固体总质量减少,二氧化锰质量不变;过氧化氢在二氧化锰做催化剂的条件下生成水和氧气,要注意配平;故答案为:A;变大;2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑;
点评 本考点主要考查了仪器的名称、气体的制取装置和收集装置的选择,同时也考查了化学方程式的书写和检查装置的气密性等,综合性比较强.气体的制取装置的选择与反应物的状态和反应的条件有关;气体的收集装置的选择与气体的密度和溶解性有关.本考点是中考的重要考点之一,主要出现在实验题中.

练习册系列答案
相关题目
11.如表实验中,对应的现象以及结论都正确且两者具有因果关系的是( )
| 选项 | 实验 | 现象 | 结论 |
| A | 将硝酸铵固体加入水中 | 溶液温度降低 | 该反应吸热 |
| B | 将一根未打磨的铝条放入硫酸铜溶液中 | 无紫红色固体析出 | 铝不如铜活泼 |
| C | 将二氧化碳通入紫色石蕊溶液中 | 紫色石蕊溶液变成红色 | 二氧化碳显酸性 |
| D | 高温下,将CO通过氧化铁粉末 | 红色粉末变为黑色 | CO具有还原性 |
| A. | A | B. | B | C. | C | D. | D |
8.我国1993年研制成功一种由相对原子质量为18,质子数为8的氧原子构成的双原子分子的气体.下列说法不正确的是( )
| A. | 这种氧原子的核外电子数为8 | B. | 这种气体由氧元素组成 | ||
| C. | 这种氧原子的中子数为10 | D. | 这种气体里氧元素的化合价不是零 |
15.一质量的某物质充分燃烧,消耗64gO2,同时生成了44gCO2和36gH2O,则该物质中( )
| A. | 只含有碳元素 | |
| B. | 只含有碳、氢两种元素 | |
| C. | 一定含有碳、氢、氧三种元素 | |
| D. | 一定含有碳、氢两种元素,可能含有氧元素 |
12.逻辑推理是一种重要的化学思维方法,以下推理正确的是( )
| A. | 离子是带电的粒子,所以带电的粒子一定是离子 | |
| B. | 单质中只含有一种元素,因此只含有一种元素的物质一定是单质 | |
| C. | 分子可以构成物质,但物质不都由分子构成 | |
| D. | 中和反应生成盐和水,由此推断生成盐和水的反应一定是中和反应 |
9.下列历史典故,涉及化学变化的是( )
| A. | 楚霸王破釜沉舟 | B. | 周都督火烧赤壁 | C. | 武老太铁杵磨针 | D. | 司马光砸缸救人 |
16.不属于新能源开发和利用的是( )
| A. |  火力发电 | B. |  风力发电 | ||
| C. |  氢燃料客车 | D. |  太阳能电池路灯 |
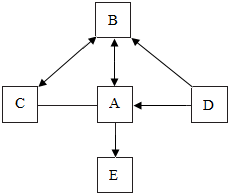 已知A、B、C、D、E是初中化学常见的五种不同物质,A、E是空气中常见的气体,其中A在空气中的含量为21%,B在常温下为液体.(说明:“-”表示相连的两种物质能发生化学反应,“→”表示相连的两种物质能向箭头所指方向转化“?”表示相连的两种物质能相互转化).试根据如图所示的关系回答下列问题:
已知A、B、C、D、E是初中化学常见的五种不同物质,A、E是空气中常见的气体,其中A在空气中的含量为21%,B在常温下为液体.(说明:“-”表示相连的两种物质能发生化学反应,“→”表示相连的两种物质能向箭头所指方向转化“?”表示相连的两种物质能相互转化).试根据如图所示的关系回答下列问题: