题目内容
19.如图是a、b、c三种物质的溶解度曲线,下列分析不解正确的是( )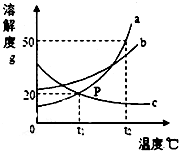
| A. | t2℃时,a、b、c三种物质的溶解度由大到小的顺序是a>b>c | |
| B. | 将t2℃时,a、b、c三种物质的饱和溶液降温至t1℃,所得溶液的溶质质量分数关系是b>a=c | |
| C. | t2℃时,将50ga物质(不含结晶水)放入1OOg水中充分溶解得到a的饱和溶液 | |
| D. | 将c的饱和溶液变为不饱和溶液,可采用降温的方法 |
分析 根据固体的溶解度曲线可以:①查出某物质在一定温度下的溶解度,从而确定物质的溶解性,②比较不同物质在同一温度下的溶解度大小,从而判断饱和溶液中溶质的质量分数的大小,③判断物质的溶解度随温度变化的变化情况,从而判断通过降温结晶还是蒸发结晶的方法达到提纯物质的目的.
解答 解:A、通过分析溶解度曲线可知,t2℃时,a、b、c三种物质的溶解度由大到小的顺序是a>b>c,故A正确;
B、t1℃时,b物质的溶解度最大,a物质次之,a、b物质的溶解度随温度的降低而减小,会析出晶体,c物质的降低温度,不会析出晶体,应该按照t2℃时减小计算,所以将t2℃时,a、b、c三种物质的饱和溶液降温至t1℃,所得溶液的溶质质量分数关系是b>a>c,故B错误;
C、t2℃时,a物质的溶解度是50g,所以将50ga物质(不含结晶水)放入1OOg水中充分溶解得到a的饱和溶液,故C正确;
D、c物质的溶解度随温度的降低而减小,所以将c的饱和溶液变为不饱和溶液,可采用降温的方法,故D正确.
故选:B.
点评 本题难度不是很大,主要考查了固体的溶解度曲线所表示的意义,及根据固体的溶解度曲线来解决相关的问题,从而培养分析问题、解决问题的能力.

练习册系列答案
相关题目
7.下列关于碳及其化合物的说法,正确的是( )
| A. | 金刚石和石墨由于碳原子排列方式不同,所以物理性质有很大差异 | |
| B. | CO和CO2都能与NaOH溶液反应 | |
| C. | CO2的排放是导致酸雨形成的原因之一 | |
| D. | 在室内放一盆澄清石灰水可防止CO中毒 |
4.在元旦联欢晚会上,化学老师表演了“吹气生火”的魔术,用棉花将淡黄色的过氧化钠(Na2O2)固体包在其中,将一根长玻璃管插入棉花团中吹气,棉花团剧烈燃烧起来.为了揭开魔术的秘密,同学们进行了如下探究.
【提出问题】过氧化钠与人呼出的哪种气体发生反应?
【查阅资料】
①人呼出的气体中主要成分是N2、O2、CO2和水蒸气等.
②NaOH溶液能与CO2反应但与O2不反应.
【作出猜想】
①过氧化钠与人呼出的N2反应并生成O2.
②过氧化钠与人呼出的水蒸气反应并生成O2.
③过氧化钠与人呼出的CO2反应并生成O2.
【进行实验】
【解释与结论】
(1)实验1中,观察到燃着的木条熄灭,可判断猜想①不成立.
(2)实验2中,A装置中发生的变化是物理(填“物理变化”或“化学变化”).
(3)实验3中,B装置所盛试剂及其作用是吸收多余的二氧化碳.
(4)由上述3个实验可判断,猜想②、③成立.已知实验2中另一种产物由3种元素组成,写出该反应的化学方程式2Na2O2+2H2O═4NaOH+O2↑.
【反思与评价】
与学过的实验室制氧气相比,过氧化钠更适合在潜水艇中使用,其优点是反应在常温下就能进行,能将二氧化碳处理掉.
【提出问题】过氧化钠与人呼出的哪种气体发生反应?
【查阅资料】
①人呼出的气体中主要成分是N2、O2、CO2和水蒸气等.
②NaOH溶液能与CO2反应但与O2不反应.
【作出猜想】
①过氧化钠与人呼出的N2反应并生成O2.
②过氧化钠与人呼出的水蒸气反应并生成O2.
③过氧化钠与人呼出的CO2反应并生成O2.
【进行实验】
| 序号 | 实验装置 | 实验现象 |
| 实验1 | 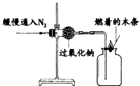 | / |
| 实验2 |  | 带火星的木条复燃 |
| 实验3 | 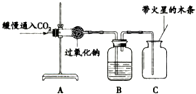 | 带火星的木条复燃 |
(1)实验1中,观察到燃着的木条熄灭,可判断猜想①不成立.
(2)实验2中,A装置中发生的变化是物理(填“物理变化”或“化学变化”).
(3)实验3中,B装置所盛试剂及其作用是吸收多余的二氧化碳.
(4)由上述3个实验可判断,猜想②、③成立.已知实验2中另一种产物由3种元素组成,写出该反应的化学方程式2Na2O2+2H2O═4NaOH+O2↑.
【反思与评价】
与学过的实验室制氧气相比,过氧化钠更适合在潜水艇中使用,其优点是反应在常温下就能进行,能将二氧化碳处理掉.
11. 研究和控制化学反应条件对工农业生产有重要意义.快乐化学小组的同学想探究双氧水的浓度对反应速率的影响.在其他条件相同的情况下进行了三次实验,记录各收集一瓶相同体积氧气所需要的时间.
研究和控制化学反应条件对工农业生产有重要意义.快乐化学小组的同学想探究双氧水的浓度对反应速率的影响.在其他条件相同的情况下进行了三次实验,记录各收集一瓶相同体积氧气所需要的时间.
(1)本实验采用的科学研究方法是控制变量法.
(2)实验3中,加入的二氧化锰质量为5g.
(3)相同条件下,实验3产生氧气的速率最快,说明双氧水的浓度越大,反应速率越快.
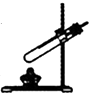
(4)有同学通过查阅资料得知,双氧水在70℃以上会较快分解产生氧气.为了验证加热双氧水也可以产生氧气,同学们选择如图装置(气密性良好)进行实验.实验中观察到试管内产生气泡,但将带火星的木条放在导管口没有复燃,可能是加热时,水蒸气会与氧气一起逸出,使木条不能复燃.同学分析原因后,采用了排水法收集气体,再检验,证明加热双氧水也可以产生氧气.
(5)加热液体时试管口向上倾斜,加热固体物质时试管口应向下倾斜,原因是防止冷凝水倒流入试管,将试管炸裂.
 研究和控制化学反应条件对工农业生产有重要意义.快乐化学小组的同学想探究双氧水的浓度对反应速率的影响.在其他条件相同的情况下进行了三次实验,记录各收集一瓶相同体积氧气所需要的时间.
研究和控制化学反应条件对工农业生产有重要意义.快乐化学小组的同学想探究双氧水的浓度对反应速率的影响.在其他条件相同的情况下进行了三次实验,记录各收集一瓶相同体积氧气所需要的时间. | 实验 | 双氧水的质量(g) | 双氧水的浓度(%) | 二氧化锰质量(g) | 收集时间(s) |
| 1 | 50 | 6 | 5 | 200 |
| 2 | 50 | 12 | 5 | 100 |
| 3 | 50 | 18 | 5 | 67 |
(2)实验3中,加入的二氧化锰质量为5g.
(3)相同条件下,实验3产生氧气的速率最快,说明双氧水的浓度越大,反应速率越快.
(4)有同学通过查阅资料得知,双氧水在70℃以上会较快分解产生氧气.为了验证加热双氧水也可以产生氧气,同学们选择如图装置(气密性良好)进行实验.实验中观察到试管内产生气泡,但将带火星的木条放在导管口没有复燃,可能是加热时,水蒸气会与氧气一起逸出,使木条不能复燃.同学分析原因后,采用了排水法收集气体,再检验,证明加热双氧水也可以产生氧气.
(5)加热液体时试管口向上倾斜,加热固体物质时试管口应向下倾斜,原因是防止冷凝水倒流入试管,将试管炸裂.
8.下列关于空气的说法中,错误的是( )
| A. | 按质量计算,空气中约含氮气78%,氧气21%,其他气体和杂质约占1% | |
| B. | 少量有害气体进入空气中,依靠大自然的自净能力,空气仍能保持洁净 | |
| C. | 空气是一种十分重要的天然资源 | |
| D. | 空气中的稀有气体一般不跟其他物质反应,曾被称为“惰性气体” |
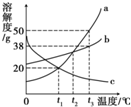 如图是a、b、c三种物质的溶解度曲线.根据图回答:
如图是a、b、c三种物质的溶解度曲线.根据图回答: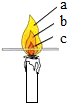 在对蜡烛及其燃烧进行了探究以后,请你填写下列空格:
在对蜡烛及其燃烧进行了探究以后,请你填写下列空格: