题目内容
将表面生锈的铁钉投入到稀盐酸中,开始时观察到铁锈逐渐减少,溶液呈棕黄色,化学方程式为 ;较长时间后观察到铁钉表面有气泡产生,化学方程式为 .
考点:书写化学方程式、文字表达式、电离方程式
专题:化学用语和质量守恒定律
分析:铁锈的主要成分是氧化铁,能与稀盐酸反应生成氯化铁与水,铁锈完全消失后,铁与稀盐酸反应生成氯化亚铁和氢气,据此写出反应的化学方程式即可.
解答:解:铁锈的主要成分是氧化铁(Fe2O3),将生锈的铁钉放入稀盐酸中,先是表面的铁锈的主要成分氧化铁与盐酸反应生成氯化铁与水,反应的化学方程式为:Fe2O3+6HCl═2FeCl3+3H2O.
当铁锈完全反应后,铁与过量的稀盐酸发生反应,生成氯化亚铁与氢气,反应的化学方程式为:Fe+2HCl═FeCl2+H2↑.
故答案为:Fe2O3+6HCl═2FeCl3+3H2O;Fe+2HCl═FeCl2+H2↑.
当铁锈完全反应后,铁与过量的稀盐酸发生反应,生成氯化亚铁与氢气,反应的化学方程式为:Fe+2HCl═FeCl2+H2↑.
故答案为:Fe2O3+6HCl═2FeCl3+3H2O;Fe+2HCl═FeCl2+H2↑.
点评:本题难度不大,考查学生根据反应原理书写化学方程式的能力,化学方程式书写经常出现的错误有不符合客观事实、不遵守质量守恒定律、不写条件、不标符号等.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
下列符号表示两个分子的是( )
| A、2H2 |
| B、H2O |
| C、2H |
| D、Cu+2 |
下列实验方案或措施中,不合理的是( )
| A、用适量稀盐酸清除铁制品表面的铁锈 |
| B、通过加水过滤除去CaO中混有的CaCO3 |
| C、用CO2鉴别NaOH溶液和Ca(OH)2溶液 |
| D、用水区分氢氧化钠固体和硝酸铵固体 |
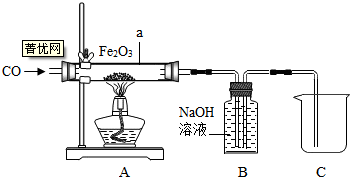
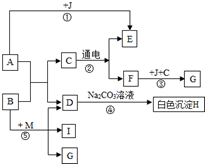 框图中A是人体胃液中含有的成分,B用于改良酸性土壤,G是铁锈的主要成分(Fe2O3),E、F、I为无色气体,其中I为有剌激性气味的气体.根据图示回答下列问题.
框图中A是人体胃液中含有的成分,B用于改良酸性土壤,G是铁锈的主要成分(Fe2O3),E、F、I为无色气体,其中I为有剌激性气味的气体.根据图示回答下列问题.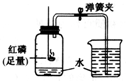 如图所示,用它来测定空气中氧气含量.点燃红磷观察到的现象是
如图所示,用它来测定空气中氧气含量.点燃红磷观察到的现象是