题目内容
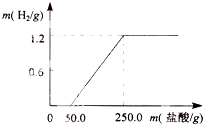 某兴趣小组从废铝锅底部剪一块铝片,将它放入21.9%的稀盐酸中,产生氢气的质量与消耗盐酸的质量如右下图(假设酸与氧化膜反应时没有H2产生,其它杂质不与酸反应).请回答:
某兴趣小组从废铝锅底部剪一块铝片,将它放入21.9%的稀盐酸中,产生氢气的质量与消耗盐酸的质量如右下图(假设酸与氧化膜反应时没有H2产生,其它杂质不与酸反应).请回答:(1)从图中看出,该反应产生了H2
(2)铝片中铝单质的质量是多少?
考点:根据化学反应方程式的计算,有关溶质质量分数的简单计算
专题:综合计算(图像型、表格型、情景型计算题)
分析:(1)图象为产生氢气质量随所加盐酸质量变化情况.根据图象可知,放出氢气质量为1.2g;
(2)由反应放出氢气的质量,根据反应的化学方程式,计算与酸反应的铝片的质量;
(2)由反应放出氢气的质量,根据反应的化学方程式,计算与酸反应的铝片的质量;
解答:解:(1)根据产生氢气的质量与消耗盐酸的质量图,可得生成氢气质量为1.2g;
(2)设生成1.2g氢气时反应的铝的质量为x
2Al+6HCl═2AlCl3+3H2↑
54 6
x 1.2g
=
x=10.8g
故答案为:(1)1.2g;
(2)铝片中铝单质的质量为10.8g;
(2)设生成1.2g氢气时反应的铝的质量为x
2Al+6HCl═2AlCl3+3H2↑
54 6
x 1.2g
| 54 |
| x |
| 6 |
| 1.2g |
x=10.8g
故答案为:(1)1.2g;
(2)铝片中铝单质的质量为10.8g;
点评:此题是对化学方程式计算的考查,解题的关键是能够利用图象得到生成的氢气的质量.

练习册系列答案
相关题目
下列实验操作中,正确的是( )
A、 |
B、 |
C、 |
D、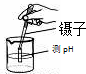 |
下列物质的用途利用了其物理性质的是( )
| A、食品包装中充氮气以防腐 |
| B、液氮用于手术时冷冻麻醉 |
| C、镁用于制照明弹 |
| D、氧气供人和动植物呼吸 |
在下列蜡烛燃烧的实验中,对有关实验现象描述错误的是( )
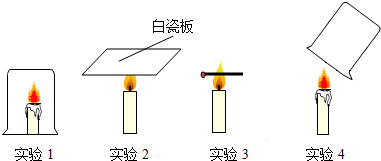

| A、实验1中蜡烛火焰逐渐熄灭 |
| B、实验2白瓷板表面无明显变化 |
| C、实验3外焰部分的火柴杆最先变黑 |
| D、实验4烧杯的内壁有水雾生成 |