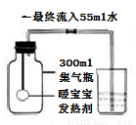
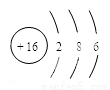
��Ŀ����
��5�֣�2012��4��15�գ����ӡ�ÿ���������桷������һЩ��ҵ��Ƥ����ϰ��ƹ�ҵ�������ڼӹ������������ظ���أ��ڼ����������ظ���طֽ⣬��Ӧ�Ļ�ѧ����ʽΪ��
4K2Cr2O7 4K2CrO4+2X+3O2������ҵ��������ҩ�ý��ң����½����ؽ��������ꡣ����һ���ؽ���Ԫ�أ��ܶԸΡ������������ٺ�DNA������ˡ���ͨ������£�������������ɫ�н�������Ĺ��壬�нϸߵ��۵㣬����Ӳ�Ľ������ڼ���ʱ������Ũ���ᷴӦ��������������и�Ԫ�ػ��ϼ�Ϊ+3�ۣ���ͬʱ������һ�ִ�����Ⱦ���һ�ֳ�����Һ�塣
4K2CrO4+2X+3O2������ҵ��������ҩ�ý��ң����½����ؽ��������ꡣ����һ���ؽ���Ԫ�أ��ܶԸΡ������������ٺ�DNA������ˡ���ͨ������£�������������ɫ�н�������Ĺ��壬�нϸߵ��۵㣬����Ӳ�Ľ������ڼ���ʱ������Ũ���ᷴӦ��������������и�Ԫ�ػ��ϼ�Ϊ+3�ۣ���ͬʱ������һ�ִ�����Ⱦ���һ�ֳ�����Һ�塣
�ش��������⣺
��1��K2CrO4�и�Ԫ�صĻ��ϼ��� ��K2Cr2O7�ֽ�����X�Ļ�ѧʽΪ ��
��2�����ɸ����ʵ��������� ��
��3����������Ũ���ᷴӦ�Ļ�ѧ����ʽΪ ��
��4��ʳƷ��ȫ�¼����ϱ��������磺�����谷��Ⱦɫ��ͷ�ȣ��ڹ������������ɽϴ�Ӱ�졣����¼�Ҫ��ѧ��������ȷ�жϡ�����Ϊ������ʶȱ����ѧ�Ե��� ������ĸ��ţ���
A��ʹ���˻�ѧ���Ӽ���ʳƷ�����嶼��Σ��
B�������谷���յ��졢��ȩ���ǻ�����Ʒ��ʳƷ��ȫ�¼����ǻ�ѧ�ǵû�
C�����ʶ������Ӱ�����������йأ�������������ʱ�
D��Ҫ������ʳ��ʹ�����и��ֳ�������Ԫ�ر�����֧ƽ��
��1��+6��1�֣� Cr2O3��1�֣���2������ɫ�н�������Ĺ��壬�۵�ϸߣ�������Ӳ�����
��3��2Cr + 6H2SO4��Ũ��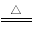 Cr2(SO4)3 + 3SO2�� + 6H2O��1�֣�4)A B
Cr2(SO4)3 + 3SO2�� + 6H2O��1�֣�4)A B
��������
�����������1����Cr�Ļ��ϼ�ΪX����ʽΪ��+1����2+X+(-2) ��4=0����X=+6�����ݻ�ѧ��Ӧǰ��ԭ�������ԭ����Ŀ�����֪��X�Ļ�ѧʽΪCr2O3����2�������ʵ����������У�����ɫ�н�������Ĺ��壬�۵�ϸߣ�������Ӳ�����3��������Ŀ����Ϣ֪����������Ũ���ᷴӦ�Ļ�ѧ����ʽΪ2Cr + 6H2SO4��Ũ�� Cr2(SO4)3 + 3SO2��+ 6H2O����4��A��ʹ���˻�ѧ���Ӽ���ʳƷ����һ�������嶼��Σ����ֻҪ����ʹ�ã�����Ӱ�����彡��������B��ʳƷ��ȫ�¼������ǶԻ�ѧ���ʵIJ�����������ɵģ��뻯ѧ�����أ�����C�����ʶ������Ӱ�����������йأ�������������ʱ䣬��ȷ��D��Ҫ������ʳ��ʹ�����и��ֳ�������Ԫ�ر�����֧ƽ�⣬��ȷ����ѡAB
Cr2(SO4)3 + 3SO2��+ 6H2O����4��A��ʹ���˻�ѧ���Ӽ���ʳƷ����һ�������嶼��Σ����ֻҪ����ʹ�ã�����Ӱ�����彡��������B��ʳƷ��ȫ�¼������ǶԻ�ѧ���ʵIJ�����������ɵģ��뻯ѧ�����أ�����C�����ʶ������Ӱ�����������йأ�������������ʱ䣬��ȷ��D��Ҫ������ʳ��ʹ�����и��ֳ�������Ԫ�ر�����֧ƽ�⣬��ȷ����ѡAB
���㣺��ѧʽ�뻯�ϼ۵ļ��㣬�����غ㶨�ɵ�Ӧ�ã���ѧ�����彡����

��12�֣���ʮһ�����Ǻ��������õ����ͣ�����ʵʩ�����������ս���γ��µķ�չ��֣�����ѧ��Դ���ۺ����ý����ص㷢չ����֮һ��
��1����ˮɹ�Σ�����ˮ���������أ�����ɹ������һ���̶�ʱ������ᾧ�أ�������ɹ����ˮ�ͻ��Ϊʳ�εı�����Һ����ɹ�ͻ����������Σ�ʣ���Һ���ΪĸҺ��Ҳ��±ˮ����
1L��ˮ����Ũ�������в����������ε��������������λ��g����ϵ���±���ʾ��
��ˮ�ܶȣ�g/mL�� | CaSO4 | NaCl | MgCl2 | MgSO4 |
1.20 | 0.91 | |||
1.21 | 0.05 | 3.26 | 0.004 | 0.008 |
1.22 | 0.015 | 9.65 | 0.01 | 0.04 |
1.26 | 0.01 | 2.64 | 0.02 | 0.02 |
1.31 | 1.40 | 0.54 | 0.03 |
I����ˮɹ���� ��ѡ���������ѧ�����仯������������ �ȹ��̡�
II�����õ����ȽϸߵĴ��κͺ�Ũ�Ƚϸߵ�±ˮ��±ˮ���ܶ�Ӧ������ʲô��Χ ��ԭ���� ��
III����ȥ���������������ʣ�Ҫ�����ܽ⡢ �� ������������
��2����ˮ��þ����ˮɹ�κ�����ĸҺ��±ˮ���ͱ��ǣ���Ҫ�ɷ���CaCO3��Ϊԭ����þ���乤����������ͼ��ʾ��

I����������ӵļ�Ӧ���� ��ѡ��������ơ���ʯ���顱��������ڷ�Ӧ�Ļ�ѧ����ʽ�� ����Ҫ��֤þ������ͭ�Ļ��˳��ѡ����˿��Ҫѡ�� �� ������Һ��
II��Mg(OH)2���ȷֽ�����MgO��H2O��MgO�Ǹ��۵�Ļ����ijЩ��ȼ�����谭ȼ�յ����ʣ�����Ч�ɷ���Mg(OH)2������ΪMg(OH)2�ܹ���ȼ��ԭ������� ��ѡ����ţ�
A��Mg(OH)2�ֽ���Ҫ���մ������ȣ������˿�ȼ����Ż��
B�����ɵ�����þ�����ڿ�ȼ����棬�����˿���
C�����ɵ�ˮ���������˿�ȼ����Χ����Ũ��
D����Ӧ�����Ƚ����˻����¶ȣ�ʹ��ȼ�ﲻ�״ﵽ�Ż��