题目内容
(1)欲配制50g 8%的硫酸铜溶液,需要硫酸铜 g,水 mL;
(2)若将溶质质量分数20%的硫酸铜溶液用水稀释成50g 8%的硫酸铜溶液,请你计算稀释所需水的质量.
(2)若将溶质质量分数20%的硫酸铜溶液用水稀释成50g 8%的硫酸铜溶液,请你计算稀释所需水的质量.
考点:有关溶质质量分数的简单计算,用水稀释改变浓度的方法
专题:溶液的组成及溶质质量分数的计算
分析:(1)利用溶质质量=溶液质量×溶质的质量分数,可根据溶液的质量和溶质的质量分数计算配制溶液所需要的溶质的质量;再根据溶剂质量=溶液质量-溶质质量即可求得水的质量.
(2)根据溶液稀释前后,溶质的质量不变,结合题意进行分析解答.
(2)根据溶液稀释前后,溶质的质量不变,结合题意进行分析解答.
解答:解:(1)溶质质量=溶液质量×溶质的质量分数,配制50g 8%的硫酸铜溶液,需要硫酸铜的质量=50g×8%=4g;溶剂质量=溶液质量-溶质质量,则所需水的质量=50g-4g=46g(合46mL).
(2)设稀释前溶液的质量为x,由溶液稀释前后,溶质的质量不变,
50g×8%=x×20% x=20g
需要水的质量为:50g-20g=30g.
故答案为:(1)4;46;(2)稀释需要水的质量为30g.
(2)设稀释前溶液的质量为x,由溶液稀释前后,溶质的质量不变,
50g×8%=x×20% x=20g
需要水的质量为:50g-20g=30g.
故答案为:(1)4;46;(2)稀释需要水的质量为30g.
点评:本题难度不大,掌握溶质质量分数的有关计算、溶液稀释前后溶质的质量不变是正确解答本题的关键.

练习册系列答案
相关题目
下列Na、Na+二种粒子的判断中不正确的是( )
①核电荷数相同 ②核外电子数相等 ③电子层结构完全相同④质量几乎相等 ⑤质子数相等 ⑥Na+比Na稳定.
①核电荷数相同 ②核外电子数相等 ③电子层结构完全相同④质量几乎相等 ⑤质子数相等 ⑥Na+比Na稳定.
| A、①④⑤ | B、①③⑤⑥ |
| C、①④⑤⑥ | D、②③ |
如图实验操作中,正确的是( )
A、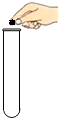 |
B、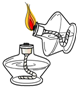 |
C、 |
D、 |
下列说法能体现物质物理性质的是( )
| A、镁粉用作照明弹 |
| B、铜丝用作导线 |
| C、氢气用作清洁燃料 |
| D、红磷用作发令枪 |
正确读写化学符号是学好化学的基础,下列读法或写法正确的是( )
| A、2Mg+2-2个镁离子 |
| B、3H2-3个氢分子 |
| C、二氧化碳-20C |
| D、氧化铁-Fe3O4 |
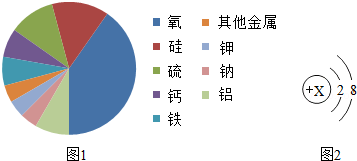 通过化学启蒙学习,同学们对组成万物的基本物质有了进一步了解.图1是某陨石样品中各种元素含量的比例图.
通过化学启蒙学习,同学们对组成万物的基本物质有了进一步了解.图1是某陨石样品中各种元素含量的比例图.