题目内容
11.如图图象能正确反映其对应关系的是( )| A. |  某温度下,向一定量接近饱和的硝酸钾溶液中不断加入过量的硝酸钾晶体 | |
| B. |  向稀盐酸和氯化钙的混合溶液中加入过量的碳酸钠溶液 | |
| C. |  向氢氧化钠溶液中滴加过量的稀盐酸 | |
| D. |  向盛有氧化铜的烧杯中加入稀盐酸至过量,生成氯化铜质量与加入稀盐酸质量的关系 |
分析 A、饱和溶液和不饱和溶液之间可以相互转化;
B、碳酸钠能和稀盐酸反应生成氯化钠、水和二氧化碳,能和氯化钙反应生成碳酸钙沉淀和氯化钠,稀盐酸能和碳酸钙反应生成氯化钙、水和二氧化碳;
C、氢氧化钠溶液显碱性,pH大于7,能和稀盐酸反应生成氯化钠和水,稀盐酸显酸性,pH小于7;
D、氧化铜和稀盐酸反应生成氯化铜和水.
解答 解:A、某温度下,向一定量接近饱和的硝酸钾溶液中不断加入过量的硝酸钾晶体的过程中,溶质质量分数增大,当达到饱和时,溶质质量分数不再增大,该选项不正确;
B、向稀盐酸和氯化钙的混合溶液中加入过量的碳酸钠溶液时,碳酸钠先和稀盐酸反应生成氯化钠、水和二氧化碳,即开始时不产生沉淀,该选项不正确;
C、向氢氧化钠溶液中滴加过量的稀盐酸时,稀盐酸和氢氧化钠反应生成氯化钠和水,溶液的碱性减弱,pH降低,恰好完全反应时,溶液显中性,pH=7,继续加入稀盐酸时,溶液显酸性,pH小于7,该选项正确;
D、向盛有氧化铜的烧杯中加入稀盐酸至过量的过程中,生成氯化铜的质量增大,当氧化铜完全反应后,氯化铜的质量不再增大,该选项不正确.
故选:C.
点评 本题主要考查物质的性质,解答时要根据各种物质的性质,结合图中信息进行分析、判断,从而得出正确的结论.

练习册系列答案
相关题目
1.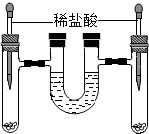 如图,将等质量的锌和铁分别加入左、右试管中,加入等质量、等质量分数的稀盐酸,充分反应后,冷却到室温,金属均有剩余,(U型管内为水,初始液面相平,反应过程中装置气密性良好)下列说法正确的是( )
如图,将等质量的锌和铁分别加入左、右试管中,加入等质量、等质量分数的稀盐酸,充分反应后,冷却到室温,金属均有剩余,(U型管内为水,初始液面相平,反应过程中装置气密性良好)下列说法正确的是( )
 如图,将等质量的锌和铁分别加入左、右试管中,加入等质量、等质量分数的稀盐酸,充分反应后,冷却到室温,金属均有剩余,(U型管内为水,初始液面相平,反应过程中装置气密性良好)下列说法正确的是( )
如图,将等质量的锌和铁分别加入左、右试管中,加入等质量、等质量分数的稀盐酸,充分反应后,冷却到室温,金属均有剩余,(U型管内为水,初始液面相平,反应过程中装置气密性良好)下列说法正确的是( )| A. | 左、右试管中溶液都会变为浅绿色 | B. | 两试管中所得溶液的质量相等 | ||
| C. | U型管中液面左升右降 | D. | U型管中液面仍相平 |
2.如图是模拟海水制盐的流程
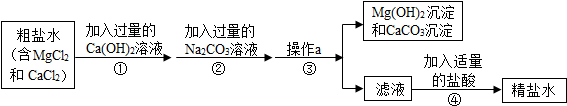
操作a的名称是过滤,所需要的玻璃仪器有漏斗(只写其中一种玻璃仪器).
【提出问题】滤液中除了含有氯化钠外,还含有哪些溶质?
【提出猜想】根据实验①②③的操作后,作出如下猜想
猜想一:由于在②中加入了过量的碳酸钠,所以滤液中除了含有氯化钠外,还仅含过量的碳酸钠.
猜想二:由于在①加入了过量的氢氧化钙,发生反应生成了氢氧化镁和氯化钙,所以滤液中除了含有氯化钠外,只含有反应生成的氯化钙.
猜想三:由于②所加的过量碳酸钠在①之后,所加的碳酸钠把①中反应生成的氯化钙和过量的氢氧化钙全部除去,所以滤液中除了含有氯化钠外,还含有氢氧化钠和碳酸钠.
【验证猜想】
【反思与拓展】为了使制得的精盐水只含有氯化钠,步骤④的作用是除去杂质,请写出其中一个反应的化学方程式:NaOH+HCl═NaCl+H2O.如果要将精盐水继续提纯成NaCl晶体,应进行蒸发结晶操作.
组成探究】
纯碱也是一种较为重要的基础化工原料,某才同学们为了测定某纯碱样品(混有少量氯化纳)的纯度,设计了如下实验:

根据实验数据,计算该纯碱样品中碳酸钠的质量分数是多少?(写出计算过程)

操作a的名称是过滤,所需要的玻璃仪器有漏斗(只写其中一种玻璃仪器).
【提出问题】滤液中除了含有氯化钠外,还含有哪些溶质?
【提出猜想】根据实验①②③的操作后,作出如下猜想
猜想一:由于在②中加入了过量的碳酸钠,所以滤液中除了含有氯化钠外,还仅含过量的碳酸钠.
猜想二:由于在①加入了过量的氢氧化钙,发生反应生成了氢氧化镁和氯化钙,所以滤液中除了含有氯化钠外,只含有反应生成的氯化钙.
猜想三:由于②所加的过量碳酸钠在①之后,所加的碳酸钠把①中反应生成的氯化钙和过量的氢氧化钙全部除去,所以滤液中除了含有氯化钠外,还含有氢氧化钠和碳酸钠.
【验证猜想】
| 步骤 | 实验操作 | 实验现象 | 结论 |
| 1 | 取少量滤液于试管中,加入过量的氯化钙溶液,振荡,静置 | 产生白色沉淀 | 猜想三是正确的 |
| 2 | 取步骤1反应后的混合液过滤后,取滤液少量于试管中加入无色酚酞试液(填指示剂) | 溶液变红色 |
组成探究】
纯碱也是一种较为重要的基础化工原料,某才同学们为了测定某纯碱样品(混有少量氯化纳)的纯度,设计了如下实验:

根据实验数据,计算该纯碱样品中碳酸钠的质量分数是多少?(写出计算过程)
19.下列有关物质的检验、鉴别、除杂、分离所用的试剂或方法正确的是( )
| 选项 | 实验目的 | 所用试剂或方法 |
| A | 检验一瓶气体是否为CO2 | 燃着的木条 |
| B | 鉴别氢氧化钠溶液和饱和石灰水 | 升高温度 |
| C | 分离铁粉和铜粉混合物 | 稀硫酸 |
| D | 除去NaOH溶液中的Na2CO3 | 氢氧化钙溶液 |
| A. | A | B. | B | C. | C | D. | D |
3.区分下列各组物质的两种方法都正确的是( )
| 需区分物质 | 方法一 | 方法二 | |
| A | 食盐和纯碱 | 闻气味 | 测pH |
| B | 黄铜和黄金 | 观察颜色 | 用稀盐酸 |
| C | 碳酸氢铵和磷矿粉 | 加水溶解 | 加熟石灰研磨 |
| D | 氢氧化钙和氢氧化钠 | 加酚酞溶液 | 通入二氧化碳 |
| A. | A | B. | B | C. | C | D. | D |
20.下表各物质都含有少量杂质,分别写出除去杂质应选用的物质及所发生的化学反应方式程式.
| 物质 | 杂质 | 除杂质选用的物质 | 发生反应的化学方程式 |
| 稀盐酸 | 稀H2SO4 | ||
| CO | CO2 | ||
| NaCl | Na2CO3 |
5.下列除去杂质的方法错误的是( )
| 选项 | 物质(括号内为杂质) | 除去杂质的方法 |
| A | CO2(CO) | 通过NaOH溶液 |
| B | N2(O2) | 通过灼热的铜网 |
| C | CaCl2(CaCO3) | 加水、过滤、蒸发 |
| D | CaO(CaCO3) | 高温煅烧 |
| A. | A | B. | B | C. | C | D. | D |
