题目内容
17.某校化学课外活动小组在一次活动中,取刚降到地面的雨水水样,每隔5分钟用pH计测定一次pH,其数据如下表:| 测定时刻 | 6:05 | 6:10 | 6:15 | 6:20 | 6:25 | 6:30 |
| p H | 4.95 | 4.94 | 4.94 | 4.88 | 4.86 | 4.85 |
(2)所取的雨水是否为酸雨?是 (填“是”或“否”);在测定的期间,雨水水样的酸性随着时间的变化逐渐增强 (填“增强”或“减弱”).
(3)经调查,这一地区有一座燃煤发电厂(生产过程中产生SO2),某同学设计用烧碱来吸收生产过程中产生的SO2,将其转化成亚硫酸钠(Na2SO3).请你帮他写出该反应的化学方程式:SO2+2NaOH═Na2SO3+H2O.
(4)“碱雨”是人们向植物施铵态氮肥时,某些干旱地区土壤多呈碱性,使铵态氮肥转化为氨气进入大气,氨气遇雨水而降,形成“碱雨”(雨水呈碱性).写出 NH4Cl与Ca(OH)2共热反应的化学方程式2NH4Cl+Ca(OH)2$\frac{\underline{\;\;△\;\;}}{\;}$CaCl2+2NH3↑+2H2O:
分析 (1)正常的空气中含有酸性气体二氧化碳易溶于水生成碳酸;
(2)pH<5.6的雨水称为酸雨,根据题中信息解答;当溶液的pH<7时,随着pH的减小酸性增强;
(3)根据反应物和生成物及其质量守恒定律可以书写化学方程式;
(4)根据反应物和生成物及其质量守恒定律可以书写化学方程式.
解答 解:(1)空气中含有二氧化碳,二氧化碳溶于水生成碳酸,而碳酸呈酸性,所以正常雨水的pH约为5.6,所发生的反应的化学方程式为:CO2+H2O═H2CO3;
(2)雨水的pH小于5.6,属于酸雨,在测定的期间,雨水水样的pH逐渐减小,酸性增强.故填:是;增强.
(3)二氧化硫和氢氧化钠反应生成亚硫酸钠和水,反应的化学方程式为:SO2+2NaOH═Na2SO3+H2O;
(4)NH4Cl与Ca(OH)2共热反应生成氯化钙、水和二氧化碳,故填:2NH4Cl+Ca(OH)2$\frac{\underline{\;\;△\;\;}}{\;}$CaCl2+2NH3↑+2H2O.
答案:
(1)CO2+H2O═H2CO3;
(2)是;增强;
(3)SO2+2NaOH═Na2SO3+H2O.
(4)2NH4Cl+Ca(OH)2$\frac{\underline{\;\;△\;\;}}{\;}$CaCl2+2NH3↑+2H2O
点评 解答本题要掌握化学方程式的书写方法以及形成酸雨的条件等方面的知识,只有这样才能对相关方面的问题做出增强的判断.

练习册系列答案
相关题目
5.下列各组离子能在指定溶液中大量共存的一组是( )
| A. | 在稀盐酸中:Ba2+、SO42-、Zn2+ | B. | 在氢氧化钙溶液中:H+、CO32-、Cl- | ||
| C. | 在氯化钠溶液中:Fe3+、Zn2+、NO3- | D. | 在氯化铵溶液中:Na+、Mg2+、OH- |
2.下列有关碳及其氧化物的说法不正确的是( )
| A. | 进入菜窖前要做灯火实验,是因为CO2有毒性 | |
| B. | CO2与CO的化学性质不同,是因为分子的构成不同 | |
| C. | 金刚石可用于切割玻璃 | |
| D. | 铅笔芯中含有石墨 |
9.关于“舌尖上的化学”,下列说法不科学的是( )
| A. | 为了身体健康,必须均衡膳食 | |
| B. | 霉变大米不可食用 | |
| C. | 为延长食品保质期,海鲜可用甲醛浸泡 | |
| D. | 为使发面食品松软可口,制作时可添加适量碳酸氢钠 |
6.下列保护自然资源的措施错误的是( )
| A. | 为防治空气污染,应加强工业废气处理 | |
| B. | 为节约用水,用工业废水直接浇灌农田 | |
| C. | 为节约化石燃料,应开发和使用新能源 | |
| D. | 为防止铁制品生锈,常在其表面覆盖保护层 |
7.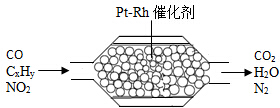 如图表示汽车尾气净化器处理汽车尾气的过程,其主要反应原理为2NO+2CO═2CO2+N2有关叙述不正确的是( )
如图表示汽车尾气净化器处理汽车尾气的过程,其主要反应原理为2NO+2CO═2CO2+N2有关叙述不正确的是( )
 如图表示汽车尾气净化器处理汽车尾气的过程,其主要反应原理为2NO+2CO═2CO2+N2有关叙述不正确的是( )
如图表示汽车尾气净化器处理汽车尾气的过程,其主要反应原理为2NO+2CO═2CO2+N2有关叙述不正确的是( )| A. | CO氧化为CO2所需氧来源于NOX | |
| B. | 该反应是置换反应 | |
| C. | Pt-Rh催化剂化学反应前后质量不变 | |
| D. | 使用该净化器能减少酸雨的发生 |