题目内容
16.实验室常用下列装置来制取氧气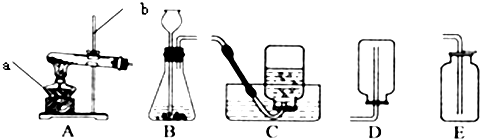
(1)写出图中有标号仪器的名称:a酒精灯、b铁架台;
(2)采用高锰酸钾制取氧气时,应选择的发生装置是A(填序号,下同),其化学反应文字表达式为高锰酸钾$\stackrel{加热}{→}$锰酸钾+二氧化锰+氧气.
(3)采用过氧化氢溶液制取氧气时,应选择的发生装置是B,锥形瓶中应先放入的药品是二氧化锰,其化学反应文字表达式为过氧化氢$\stackrel{二氧化锰}{→}$水+氧气,它与采用装置A制取氧气时比较,主要优点是节约能源(任答一条).
(4)收集氧气可以选择装置C或E,你选择它的理由是氧气不易溶于水或氧气的密度比空气大若用排水法收集氧气时,当观察到气泡均匀、连续地冒出时才开始收集,否则收集的氧气不纯.
(5)某同学收集完毕,先停止加热再将导管移出水面,你预测这种操作可能会引起的后果是水倒流入试管把试管炸裂.如果选用E收集氧气,验满的方法是把带火星的木条放在集气瓶口,如果带火星的木条复燃,说明已经收集满.
分析 (1)要熟悉各种仪器的名称、用途和使用方法;
(2)高锰酸钾受热时能够分解生成锰酸钾、二氧化锰和氧气;
(3)通常情况下,过氧化氢在二氧化锰的催化作用下,分解生成水和氧气;
(4)氧气的密度比空气的密度大,不易溶于水;
(5)利用加热的方法制取气体,并且利用排水法收集气体时,要按照一定的步骤进行,特别是要注意集满气体后的操作顺序,以防发生安全事故;
氧气能使带火星的木条复燃.
解答 解:(1)a是酒精灯,常用作热源;b是铁架台,常用于固定、支持实验装置.
故填:酒精灯;铁架台.
(2)采用高锰酸钾制取氧气时需要加热,应选择的发生装置是A;
其化学反应文字表达式为:高锰酸钾$\stackrel{加热}{→}$锰酸钾+二氧化锰+氧气.
故填:A;高锰酸钾$\stackrel{加热}{→}$锰酸钾+二氧化锰+氧气.
(3)采用过氧化氢溶液制取氧气时不需要加热,应选择的发生装置是B;
锥形瓶中应先放入的药品是二氧化锰,其化学反应文字表达式为:过氧化氢$\stackrel{二氧化锰}{→}$水+氧气;
它与采用装置A制取氧气时比较,主要优点是节约能源,产物不污染环境等.
故填:B;二氧化锰;过氧化氢$\stackrel{二氧化锰}{→}$水+氧气;节约能源.
(4)因为氧气的密度比空气大,可以用向上排空气法收集,即用E装置收集,氧气不易溶于水,可以用排水法收集,即用C装置收集;
若用排水法收集氧气时,当观察到气泡均匀、连续地冒出时才开始收集,否则收集的氧气不纯.
故填:C或E;氧气不易溶于水或氧气的密度比空气大;均匀、连续地冒出.
(5)这种操作可能会引起的后果是水倒流入试管把试管炸裂;
如果选用E收集氧气,验满的方法是:把带火星的木条放在集气瓶口,如果带火星的木条复燃,说明已经收集满.
故填:水倒流入试管把试管炸裂;把带火星的木条放在集气瓶口,如果带火星的木条复燃,说明已经收集满.
点评 本题主要考查仪器的用途、反应表达式的书写,实验装置的选择,选择发生装置时,要考虑反应物的状态、反应条件等因素;选择收集装置时,要考虑气体的水溶性、能否和水发生化学反应、密度、能否和空气中的物质发生化学反应等因素.

(1)请你仿照下表中的示例,找出CO2、CH4、C2H2(乙炔)、C2H4(乙烯)这四种气体之间存在的另外两个规律并排序.
| 规律 | 排序 |
| 示例:标准状况下,密度由大到小 | CO2、C2H4、C2H2、CH4 |
A.该气体中一定含有C2H4
B.该气体中一定没有CH4
C.该气体中可能含有C2H2
D.该气体不可能同时含有CH4、C2H2、C2H4.
| A. | 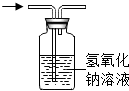 除去一氧化碳中的二氧化碳 | B. | 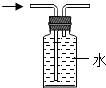 排水法收集氢气 | ||
| C. | 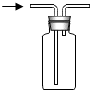 向上排空气法收集氧气 | D. |  检验氢气中是否混有氯化氢 |
| A. | 铜粉中混有铁粉(加稀硫酸后过滤) | |
| B. | CaO中混有CaCO3(高温煅烧) | |
| C. | FeSO4溶液中混有CuSO4(放入铁钉后过滤) | |
| D. | CO2中混有CO(点燃) |
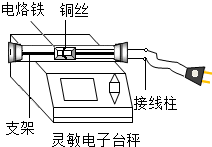 如图为小柯做的创新实验:将铜丝绕在电烙铁上,电烙铁用支架固定在密闭的硬质玻璃管中,玻璃管置于灵敏电子台秤上,接通电路,电烙铁开始工作,可以观察到铜丝表面逐渐变黑,电子台秤读数保持不变,下列说法正确的是( )
如图为小柯做的创新实验:将铜丝绕在电烙铁上,电烙铁用支架固定在密闭的硬质玻璃管中,玻璃管置于灵敏电子台秤上,接通电路,电烙铁开始工作,可以观察到铜丝表面逐渐变黑,电子台秤读数保持不变,下列说法正确的是( )| A. | 该反应的化学方程式是Cu+O2═CuO | |
| B. | 加热过程中,玻璃管内空气的质量保持不变 | |
| C. | 加热过程中,铜丝的质量保持不变 | |
| D. | 硬质玻璃管内物质在反应前后总质量保持不变 |
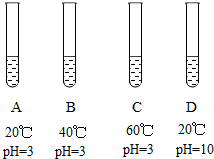 未经处理的工业废水会严重污染水和土壤,某种新型催化剂可有效降解工业废水中的有机污染物,为探究该催化剂降解有机污染物的速度都受那些因素影响,学习小组进行了如下实验.
未经处理的工业废水会严重污染水和土壤,某种新型催化剂可有效降解工业废水中的有机污染物,为探究该催化剂降解有机污染物的速度都受那些因素影响,学习小组进行了如下实验.取四份等质量的某有机物,控制条件如图,然后进入等量的新型催化剂,取得该有机物被降解的百分比随时间变化的关系如下表:
| 时间(分) 有机物被降解百分比(%) 组别 | 0 | 5 | 10 | 15 |
| A | 0 | 10 | 40 | 60 |
| B | 0 | 40 | 80 | 100 |
| C | 0 | 30 | 60 | 90 |
| D | 0 | 0 | 0 | 0 |
(1)实验中设置A和D组的目的是探究pH对降解反应速度的影响;
(2)实验A,B,C三组结果表明,当pH相等时,温度升高,降解反应速度先增大后减小(选填“先增大后减小”或“先减小后增大”);
(3)部分同学认为pH=3时,40℃是该催化剂最合适的温度,但有同学并不认同,为寻找该催化剂最合适的温度,他应该采取的做法是在40℃附近多设置几组进行实验;
(4)实验中若要测定某一时刻有机物被降解的百分比,需要迅速把试管中液体的pH调到10,这样做的目的是使反应立即停止.