题目内容
9.过氧化钙(CaO2)是一种对环境友好的多功能无机化合物,通常有两种制备方法.已知:温度过高过氧化物会分解生成氧化物和氧气.
方法1:由Ca(OH)2为原料最终反应制得,其制备流程如图1:
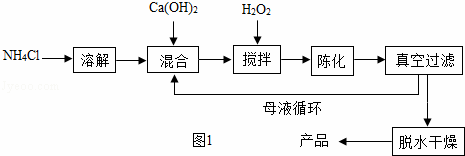
方法2:由鸡蛋壳(含CaCO3高达90%)为原料最终反应制得,其制备流程如图2:
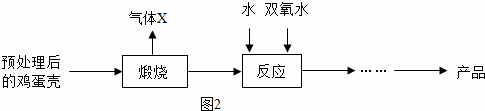
(1)请将方法1搅拌过程中发生反应的化学方程式补充完整:
CaCl2+H2O2+2NH3•H2O+6H2O═CaO2•8H2O↓+2NH4Cl.
制备过程中除水外可循环使用的物质是NH4Cl(填化学式)
(2)方法2中气体X是CO2,煅烧后的反应是化合反应,也能生成CaO2•8H2O,反应的化学方程式为CaO+7H2O+H2O2=CaO2•8H2O.该反应需控制温度在0~2℃,可将反应器放置在冰水混合物中,获得的CaO2产品中主要含有的固体杂质是Ca(OH)2(填化学式)
(3)这两种制法均要求在低温下进行(除煅烧外),温度过高会造成氨水挥发外,还能使CaO2•8H2O分解.
(4)“绿色化学”一般是指反应物的原子全部转化为期望的最终产物,则上述两种方法中生成CaO2•8H2O的反应符合“绿色化学”的是方法2(填“方法1”或“方法2”).
分析 (1)化学反应前后,元素的种类不变,原子的种类、总个数不变;
(2)高温条件下,碳酸钙分解生成氧化钙和二氧化碳;
冰水混合物能够提供0℃的温度环境;
氧化钙能和水反应生成氢氧化钙;
(3)温度过高会造成氨水挥发外,还能使CaO2•8H2O分解;
(4)根据反应的化学方程式可以判断反应是否符合“绿色化学”.
解答 解:(1)方法1搅拌过程中发生反应的化学方程式为:CaCl2+H2O2+2NH3•H2O+6H2O═CaO2•8H2O↓+2NH4Cl;
制备过程中除水外可循环使用的物质是NH4Cl.
故填:H2O;NH4Cl.
(2)方法2中气体X是CO2;
氧化钙、水、过氧化氢反应生成CaO2•8H2O,反应的化学方程式为:CaO+7H2O+H2O2=CaO2•8H2O;
该反应需控制温度在0~2℃,可将反应器放置在冰水混合物中;
获得的CaO2产品中主要含有的固体杂质是氧化钙和水反应生成的氢氧化钙.
故填:CO2;CaO+7H2O+H2O2=CaO2•8H2O;冰水混合物;Ca(OH)2.
(3)这两种制法均要求在低温下进行(除煅烧外),温度过高会造成氨水挥发外,还能使CaO2•8H2O分解.
故填:使CaO2•8H2O分解.
(4)方法2中,反应物的原子全部转化为期望的最终产物,反应符合“绿色化学”.
故填:方法2.
点评 本题主要考查物质的性质,解答时要根据各种物质的性质,结合各方面条件进行分析、判断,从而得出正确的结论.

练习册系列答案
 一线名师提优试卷系列答案
一线名师提优试卷系列答案 阳光试卷单元测试卷系列答案
阳光试卷单元测试卷系列答案
相关题目
3.材料的研制代表了一个国家的工业最高水平,我国发射的神舟十号载人飞船,采用了一种新型的材料,其中一种航天材料是以铝镁为基本材料,将石墨作为增强材料分散在其中制得的具有特殊性能的材料,它属于( )
| A. | 金属材料 | B. | 无机非金属材料 | C. | 合成材料 | D. | 复合材料 |
4.过氧化钙(CaO2)是一种多功能无机化合物,通常由Ca(OH)2为原料制得,制备流程如下.下列有关说法正确的是( )


| A. | 原料中NH4Cl中氮元素的化合价是+3 | |
| B. | 搅拌中的化学方程式:CaC12+H2O2+2NH3+8X═CaO2•8H2O↓+2NH4Cl,其中X的化学式为H2O | |
| C. | 过程中除水外可循环使用的物质是NH4C1 | |
| D. | 这种制法要求低温下进行,只是避免造成氨水挥发 |
19. 如图关于碳和碳的氧化物知识网络图【图中“→”表示转化关系,“…”表示相互能反应】说法正确的是( )
如图关于碳和碳的氧化物知识网络图【图中“→”表示转化关系,“…”表示相互能反应】说法正确的是( )
 如图关于碳和碳的氧化物知识网络图【图中“→”表示转化关系,“…”表示相互能反应】说法正确的是( )
如图关于碳和碳的氧化物知识网络图【图中“→”表示转化关系,“…”表示相互能反应】说法正确的是( )| A. | “C …CO2”的反应是放热反应 | |
| B. | “CO2?H2CO3”可用酚酞试剂验证 | |
| C. | “CO2→CaCO3”的反应可用于检验二氧化碳 | |
| D. | “CO→CO2”只能通过和金属氧化物反应实现 |
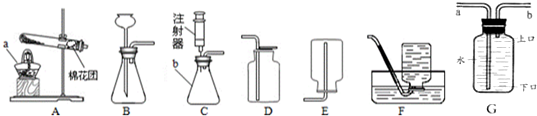
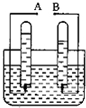 根据如图电解水的现象,请回答:
根据如图电解水的现象,请回答: