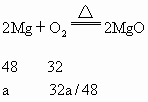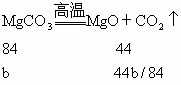题目内容
一定质量的镁和碳酸镁混合物,经高温煅烧,直到质量不再变化为止.发现反应前后总质量不变,求原混合物中镁粉的质量分数.
答案:44%
解析:
解析:
|
这里包括两个反应:
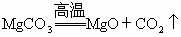
对于镁粉来说,生成物质量增加了,增加部分是反应物氧气质量.对于碳酸镁来说,生成物质量减少了,减少部分是 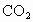 质量,且增加量等于减少量,这样不难计算. 质量,且增加量等于减少量,这样不难计算.
设在混合物中镁的质量为 a,碳酸镁的质量为b.
由于固体质量不变,根据质量守恒定律,可得镁消耗的氧气与碳酸镁生成的二氧化碳的质量相等,即 32a/48=44b/84,所以b=14a/11,则镁的质量分数为a/(a+14a/11)×100%=44%. |

练习册系列答案
 浙江名校名师金卷系列答案
浙江名校名师金卷系列答案
相关题目