题目内容
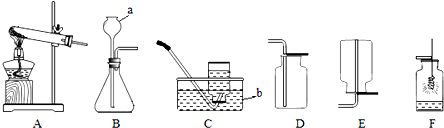
5.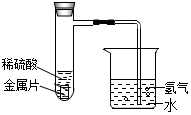 某课外活动小组设计了如图所示的实验装置,用来研究不同金属跟稀硫酸反应的快慢.他们用此装置,选择了甲、乙、丙、丁四种大小相同的金属片,分别与相同体积、相同质量分数的稀硫酸反应,在30秒钟里观察从导管口冒出的氢气泡数量,记录在表中.(“+”越多表示产生的气泡越多)
某课外活动小组设计了如图所示的实验装置,用来研究不同金属跟稀硫酸反应的快慢.他们用此装置,选择了甲、乙、丙、丁四种大小相同的金属片,分别与相同体积、相同质量分数的稀硫酸反应,在30秒钟里观察从导管口冒出的氢气泡数量,记录在表中.(“+”越多表示产生的气泡越多)| 金属 | 甲 | 乙 | 丙 | 丁 |
| 氢气泡数量 | ++ | ++++ | +++ | + |
(2)如果四种金属分别是镁、铝、铁、锌中的一种,则丁最有可能是铁.
分析 (1)利用表格中的记录可判断气泡的多少来得出金属的活泼性强弱;
(2)根据镁、铝、铁、锌的活泼性为:镁>铝>锌>铁,判断丁为铁.
解答 解:(1)气泡的多少可说明反应进行的快慢,根据表格中的记录可知:金属的活泼性为乙>丙>甲>丁;
(2)镁、铝、铁、锌的活泼性为:镁>铝>锌>铁,则丁最有可能是铁.
故答案为:(1)乙>丙>甲>丁;
(2)铁.
点评 本题主要考查了金属活动性顺序的应用,难度不大,注意在平时多加训练即可完成.

练习册系列答案
相关题目
11.在pH=1的条件下,下列溶液能大量共存,且溶液为无色的是( )
| A. | Na2CO3 KNO3 Na2SO4 | B. | H2SO4 NaCl BaCl2 | ||
| C. | Ba(NO3)2 KNO3 NaCl | D. | Na2SO4 CuSO4 NaCl |
13.下列有关现象的描述正确的是( )
| A. | 少量面粉放入足量水中充分搅拌,能形成均一、稳定的溶液 | |
| B. | 木炭在氧气中燃烧发出白光,生成黑色固体,放出热量 | |
| C. | 将Cu(OH)2加入到滴有酚酞试液的蒸馏水中,溶液显红色 | |
| D. | 把氢氧化钠溶液中逐滴加入氯化铁溶液中,产生红褐色沉淀 |
20.香料化学家已经开发出多种脂类人工香料,如丁酸甲酯(化学式为C5H10O2)具有苹果香味.下列有关丁酸甲酯的说法正确的是( )
| A. | 丁酸甲酯属于氧化物 | |
| B. | 丁酸甲酯由5个碳原子、10个氢原子和2个氧原子构成 | |
| C. | 丁酸甲酯中碳元素、氢元素和氧元素的质量比为30:5:16 | |
| D. | 丁酸甲酯的每个分子由17个原子构成 |
10.下列化学反应中,没有黑色物质生成的是( )
| A. | 加热碱式碳酸铜 | B. | 铁丝在氧气中燃烧 | ||
| C. | 加热碳铵 | D. | 加热高锰酸钾 |
14.下列实验能直接用于验证质量守恒定律的是( )
| A. | 镁条在空气中燃烧 | B. | 氢氧化钠溶液与硫酸铜溶液混合 | ||
| C. | 干冰放在密闭容器中加热 | D. | 稀盐酸滴加到盛放石灰石的烧杯中 |
15.下列实验操作正确的是( )
| A. | 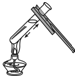 加热液体 | B. | 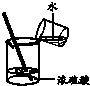 稀释浓硫酸 | C. | 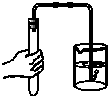 检验气密性 | D. |  熄灭酒精灯 |
 在宏观、微观和符号之间建立联系是化学学科的特点.
在宏观、微观和符号之间建立联系是化学学科的特点.