题目内容
14.油罐着火发生爆炸,消防队员用消防水龙头对油罐连续喷水,数小时后火势基本被扑灭,依据学过的化学知识,请你回答下列问题:点燃
(1)对油罐喷水的作用是使油的温度降低到它的着火点以下,防止再次燃烧.
(2)假设汽油中某一成分用X表示,燃烧时只发生如下反应:X+5O2═3CO2+4H2O,推断X的化学式为:C3H8.
分析 水在灭火中的主要作用是降低温度,根据化学反应前后原子的种类与数目不发生改变可以推出物质的化学式.
解答 解:(1)对油罐继续喷水的作用是使油的温度降低到它的着火点以下,防止再次燃烧.故填:使油的温度降低到它的着火点以下,防止再次燃烧.
(2)由X+5O2═3CO2+4H2O可知,根据质量守恒定律可知,反应前后每种原子的总数不变,由此可知,每个X中含有3个碳原子和8个氢原子,是C3H8.故填:C3H8.
点评 解答本题要掌握灭火的方法和质量守恒定律等方面的内容,只有这样才能对相关方面的问题做出正确的判断.

练习册系列答案
相关题目
4.金属镍及其化合物能发生下列反应:①Ni+2HCl=NiCl2+H2↑;②NiO+2HCl=NiCl2+H2O;③NiO2+4HCl=NiCl2+Cl2↑+2H20;分析化学方程式可知,下列说法中错误的是( )
| A. | 镍能从硫酸铜溶液中置换出铜 | |
| B. | 反应①属于复置换反应 | |
| C. | 反应③中Ni的化合价由+4价变为+2价 | |
| D. | 上述3个反应中涉及2种单质 |
5.在硝酸铜、硝酸锌、硝酸银三种物质的混合溶液里,加入过量的铁粉,充分反应后过滤,滤液中存在的金属离子是( )
| A. | Fe2+、Zn2+ | B. | Cu2+、Zn2+ | C. | Fe3+、Zn2+ | D. | Cu2+、Ag+ |
9.某化学活动小组的同学用自来水配制氢氧化钠溶液做“碱的性质”实验,结果配制几次所得的溶液都出现白色浑浊.对此现象小组同学都感到疑惑,于是进行了如下探究.
【提出问题】白色浑浊物是什么物质?
【查阅资料】①该地区自来水是硬水,常常含有Ca(HCO3)2和Mg(HCO3)2.
②Ca(HCO3)2与足量的氢氧化钠反应的化学方程式:Ca(HCO3)2+2NaOH═CaCO3↓+2H2O+Na2CO3
Mg(HCO3)2与足量的氢氧化钠反应的化学方程式:Mg(HCO3)2+2NaOH═Mg(OH)2↓+2H2O+Na2CO3
【作出猜想】猜想一:白色浑浊物是CaCO3 猜想二:白色浑浊物是Mg(OH)2
猜想三:白色浑浊物是CaCO3、Mg(OH)2
【实验探究】取氢氧化钠于烧杯中,加此自来水搅拌,静置冷却、过滤,将滤渣分为两份.
【实验反思】
(1)实验室配制溶液时应使用蒸馏水;
(2)实验②中在滤渣中加入热的蒸馏水后,滴加酚酞试液酚酞变红,冷却后红色褪去,可能的原因是氢氧化镁的溶解度随着温度的升高而增大;
【拓展延伸】
(3)将过滤后的滤液变成纯净的氢氧化钠溶液,你的方法是(用1化学方程式表示):Na2CO3+Ca(OH)2═CaCO3↓+2NaOH.
【提出问题】白色浑浊物是什么物质?
【查阅资料】①该地区自来水是硬水,常常含有Ca(HCO3)2和Mg(HCO3)2.
②Ca(HCO3)2与足量的氢氧化钠反应的化学方程式:Ca(HCO3)2+2NaOH═CaCO3↓+2H2O+Na2CO3
Mg(HCO3)2与足量的氢氧化钠反应的化学方程式:Mg(HCO3)2+2NaOH═Mg(OH)2↓+2H2O+Na2CO3
【作出猜想】猜想一:白色浑浊物是CaCO3 猜想二:白色浑浊物是Mg(OH)2
猜想三:白色浑浊物是CaCO3、Mg(OH)2
【实验探究】取氢氧化钠于烧杯中,加此自来水搅拌,静置冷却、过滤,将滤渣分为两份.
| 实验步骤 | 实验现象 | 实验结论 |
| ①取一份滤渣滴加足量稀盐酸 | 产生气泡 | 猜想三正确 |
| ②取一份滤渣加入热的蒸馏水振荡,在上层清液中再滴加无色酚酞试液 | 酚酞试液变红 |
(1)实验室配制溶液时应使用蒸馏水;
(2)实验②中在滤渣中加入热的蒸馏水后,滴加酚酞试液酚酞变红,冷却后红色褪去,可能的原因是氢氧化镁的溶解度随着温度的升高而增大;
【拓展延伸】
(3)将过滤后的滤液变成纯净的氢氧化钠溶液,你的方法是(用1化学方程式表示):Na2CO3+Ca(OH)2═CaCO3↓+2NaOH.
19.2013年“世界水日”的宣传主题是“水合作”(WaterCooperation).我国纪念2013年“世界水日”和“中国水周”活动的宣传主题为“节约保护水资源,大力建设生态文明”.下列说法错误的是( )
| A. | 水的天然循环能实现水的从新分配,不需兴建水利工程 | |
| B. | 农业生产中改变灌溉方式,变漫灌为喷灌或滴灌,以节约用水 | |
| C. | 为了避免水体污染,农业上应合理使用农药和化肥 | |
| D. | 将生活用水,地表雨水分类处理,可减少污染,保护水资源 |
6.下列通过实验得出的结论,其中不合理的是( )
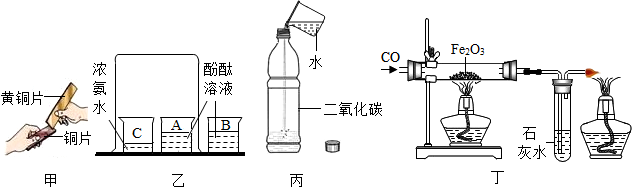

| A. | 甲实验中黄铜片能在铜片上刻画出痕迹可以说明黄铜的硬度比铜大 | |
| B. | 乙实验既可以说明分子在不停地运动着,又可以说明氨水显碱性 | |
| C. | 丙实验既可以说明二氧化碳易溶于水,又可以说明二氧化碳具有酸性 | |
| D. | 丁实验既可以说明一氧化碳具有还原性,又可以说明一氧化碳具有可燃性 |
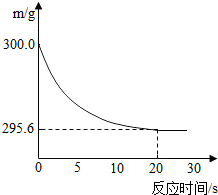 向盛有22.3g Na2CO3和NaCl固体混合物的烧杯中加入216.1g稀盐酸恰好反应,反应过程用精密仪器测得烧杯连同药品的质量(m)与反应时间(t)的关系如图所示:烧杯连同药品的起始质量为300g.求反应后,得到室温下的不饱和溶液.所得溶液中溶质的质量分数为多少?
向盛有22.3g Na2CO3和NaCl固体混合物的烧杯中加入216.1g稀盐酸恰好反应,反应过程用精密仪器测得烧杯连同药品的质量(m)与反应时间(t)的关系如图所示:烧杯连同药品的起始质量为300g.求反应后,得到室温下的不饱和溶液.所得溶液中溶质的质量分数为多少?