题目内容
17.维生素C(C6H8O6)主要存在于蔬菜水果,它能促进人体生长发育,增强人体对疾病的抵抗力,近年来科学家还发现维生素C有防癌作用.下列关于维生素C的说法错误的是( )| A. | 维生素C是有机化合物 | |
| B. | 1个维生素分子有6个碳原子,8个氢原子,6个氧原子构成 | |
| C. | 维生素C中C、H、0三种元素的质量比为3:4:3 | |
| D. | 维生素C中氢元素的质量分数为4.5% |
分析 根据维生素C的化学式C6H8O6可知,该物质由C、H、O三种元素组成,其1个分子中含6个C原子、8个H原子6个O原子共20个原子;根据化学式所传递的以上信息,完成有关化学式的计算及判断.
解答 解:A、维生素C是含有碳元素的化合物,属于有机化合物;故A说法正确;
B、根据维生素C的化学式C6H8O6可知,1个维生素C分子是由6个碳原子、8个氢原子、6个氧原子构成的;故B说法正确;
C、根据维生素C的化学式C6H8O6,维生素C中C、H、O三种元素的质量之比=(12×6):(1×8):(16×6)=9:1:12;故C说法错误;
D、根据维生素C的化学式C6H8O6可知,氢元素的质量分数为$\frac{8}{12×6+1×8+16×6}$×100%=4.5%;故D说法正确;
故选C.
点评 本题难度不大,考查同学们结合新信息、灵活运用化学式的含义与有关计算进行分析问题、解决问题的能力.

练习册系列答案
相关题目
3.下列图示实验操作正确的是( )
| A. |  点燃酒精灯 | B. | 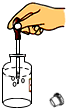 打开瓶盖吸少量液体 | ||
| C. | 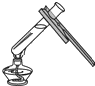 给液体加热 | D. |  滴加液体 |
4.下列属于化学变化的是( )
| A. | 冰雪消融 | B. | 酒精挥发 | C. | 食物腐烂 | D. | 活性炭除臭 |
5.小明学习完九年级化学后,对“金属与硫酸反应快慢的影响因素”进行了探究.
【提出问题】金属与硫酸反应快慢受哪些因素的影响呢?
【猜想与假设】a.可能与硫酸的浓度有关;b.可能与反应时的温度有关.
【设计并实验】小明用不同质量分数的硫酸和相同形状的锌进行如表实验.
【分析数据,得出结论】
(1)写出锌与硫酸反应的化学方程式Zn+H2SO4=ZnSO4+H2↑.
(2)通过实验①③相比,说明其它条件相同,温度越高,反应速率越快;通过实验②③或①④(写编号)说明反应物浓度对反应快慢有影响.
(3)如果硫酸质量分数为5%,温度为25℃,则收集40mL气体所需的时间范围为48s~69s.
【反思】
(1)小明在做以上四组反应时,发现一开始反应速率都很慢,原因是实验前没有除去锌表面的氧化膜.
(2)浓度相同,颗粒大小可能影响化学反应的速率,请设计实验方案进行验证在30℃时,向两支试管中分别加入5g锌粉、锌粒,再分别取20mL10%的稀盐酸,测定收集40mL气体所需的时间.
(3)影响金属与酸反应快慢的因素还有很多,请你再设计实验探究一种因素的影响.取两份相同浓度、相同体积的稀硫酸,在相同温度下,加入相同的片状的锌和铝,比较收集相同体积的氢气所需的时间.
【提出问题】金属与硫酸反应快慢受哪些因素的影响呢?
【猜想与假设】a.可能与硫酸的浓度有关;b.可能与反应时的温度有关.
【设计并实验】小明用不同质量分数的硫酸和相同形状的锌进行如表实验.
| 实验编号 | 硫酸的质量分数 (均取20mL) | 温度/℃ | 收集40mL气体所需时间/秒 |
| ① | 5% | 30 | 48 |
| ② | 10% | 20 | 41 |
| ③ | 5% | 20 | 69 |
| ④ | 10% | 30 | 32 |
(1)写出锌与硫酸反应的化学方程式Zn+H2SO4=ZnSO4+H2↑.
(2)通过实验①③相比,说明其它条件相同,温度越高,反应速率越快;通过实验②③或①④(写编号)说明反应物浓度对反应快慢有影响.
(3)如果硫酸质量分数为5%,温度为25℃,则收集40mL气体所需的时间范围为48s~69s.
【反思】
(1)小明在做以上四组反应时,发现一开始反应速率都很慢,原因是实验前没有除去锌表面的氧化膜.
(2)浓度相同,颗粒大小可能影响化学反应的速率,请设计实验方案进行验证在30℃时,向两支试管中分别加入5g锌粉、锌粒,再分别取20mL10%的稀盐酸,测定收集40mL气体所需的时间.
(3)影响金属与酸反应快慢的因素还有很多,请你再设计实验探究一种因素的影响.取两份相同浓度、相同体积的稀硫酸,在相同温度下,加入相同的片状的锌和铝,比较收集相同体积的氢气所需的时间.
2.日常生活中的一些小窍门或小常识往往包含着一些化学原理.下列做法正确的是( )
| A. | 油锅着火立即用水扑灭 | B. | 用燃烧的方法鉴别蚕丝和涤纶 | ||
| C. | 用钢丝球擦洗铝壶上的污垢 | D. | 煤气泄漏,及时打开换气扇排气 |
6.下列事故处理的方法,正确的是( )
| A. | 电路着火,用水浇 | |
| B. | 室内着火,打开所有的门窗 | |
| C. | 图书档案失火时选用二氧化碳灭火器灭火 | |
| D. | 发现煤气泄漏时,立即打开排气扇 |
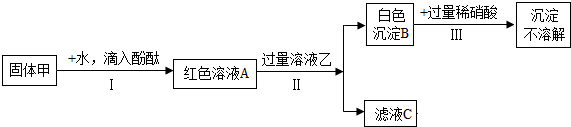
 小刚和小丽两位同学用如图所示装置进行实验,验证二氧化碳与氢氧化钠、氢氧化钙都能发生反应.
小刚和小丽两位同学用如图所示装置进行实验,验证二氧化碳与氢氧化钠、氢氧化钙都能发生反应.