题目内容
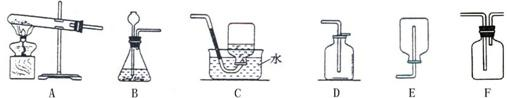
 硫化氢(H2S)是一种具有臭鸡蛋气味的致命毒气,它的密度比空气大,可溶于水形成氢硫酸,氢硫酸具有酸的通性.实验室常用固体硫化亚铁(FeS)和稀硫酸在常温下制得H2S,同时生成FeS04.
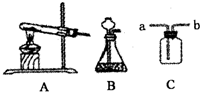
硫化氢(H2S)是一种具有臭鸡蛋气味的致命毒气,它的密度比空气大,可溶于水形成氢硫酸,氢硫酸具有酸的通性.实验室常用固体硫化亚铁(FeS)和稀硫酸在常温下制得H2S,同时生成FeS04.(1)在如图中,应选用图
(2)收集H2S气体满后,对产生尾气的处理方法是:
(3)实验室若制取6.8克的硫化氢气体,理论上需要多少克20%的硫酸溶液?
分析:(1)根据实验室制取硫化氢的反应物状态、反应条件可以选择制取硫化氢的发生装置;
(2)氢硫酸具有酸的通性,能和碱性溶液发生反应;
(3)根据反应的化学方程式、硫化氢的质量可以计算硫酸溶液的质量.
(2)氢硫酸具有酸的通性,能和碱性溶液发生反应;
(3)根据反应的化学方程式、硫化氢的质量可以计算硫酸溶液的质量.
解答:解:(1)固体硫化亚铁和稀硫酸反应时不需要加热,应该用B装置作为发生装置.
故填:B.
(2)氢氧化钠和硫化氢反应生成硫化钠和水,因此可以用氢氧化钠溶液吸收硫化氢气体.
故填:用氢氧化钠溶液吸收.
(3)解:设需要20%硫酸溶液的质量为x,
FeS+H2SO4═FeS04+H2S↑,
98 34
x×20% 6.8g
=
,
x=98g;
答:若制取6.8g的硫化氢气体,理论上需要98g20%的硫酸溶液.
故填:B.
(2)氢氧化钠和硫化氢反应生成硫化钠和水,因此可以用氢氧化钠溶液吸收硫化氢气体.
故填:用氢氧化钠溶液吸收.
(3)解:设需要20%硫酸溶液的质量为x,
FeS+H2SO4═FeS04+H2S↑,
98 34
x×20% 6.8g
| 98 |
| 34 |
| x×20% |
| 6.8g |
x=98g;
答:若制取6.8g的硫化氢气体,理论上需要98g20%的硫酸溶液.
点评:本题主要考查实验装置的选择、酸碱中和反应、根据化学方程式计算的方面的知识,计算时要注意规范性和准确性.

练习册系列答案
 名师金手指领衔课时系列答案
名师金手指领衔课时系列答案
相关题目