题目内容
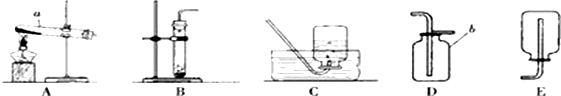
10. 医生在给病人输液时,常用葡萄糖注射液.如图是葡萄糖注射液的部分标签图
医生在给病人输液时,常用葡萄糖注射液.如图是葡萄糖注射液的部分标签图(1)葡萄糖的化学式是C6H12O6,该物质中C、H、O三种元素的质量比为6:1:8
(2)葡萄糖中碳元素的质量分数是多少?40%
(3)现要配制100千克这种葡萄糖注射液,需要葡萄糖多少千克?(写出计算过程)
分析 (1)根据化合物中各元素质量比=各原子的相对原子质量×原子个数之比,进行分析解答.
(2)根据化合物中元素的质量分数=$\frac{相对原子质量×原子个数}{相对分子质量}$×100%,进行分析解答.
(3)利用溶质质量=溶液质量×溶质的质量分数,可根据溶液的质量和溶质的质量分数计算配制溶液所需要的溶质的质量.
解答 解:(1)葡萄糖中C、H、O三种元素的质量比(12×6):(1×12):(16×6)=6:1:8.
(2)葡萄糖中碳元素的质量分数是$\frac{12×6}{12×6+1×12+16×6}×$100%=40%.
(3)现要配制100千克这种葡萄糖注射液,需要葡萄糖的质量为100kg×5%=5g.
故答案为:(1)6:1:8;(2)40%;(3)需要葡萄糖的质量为5g.
点评 本题难度不大,考查同学们结合标签新信息、灵活运用化学式与溶质质量分数的有关计算进行分析问题、解决问题的能力.

练习册系列答案
 考前必练系列答案
考前必练系列答案
相关题目
20.已知粗盐中常含有泥沙和Ca2+、Mg2+、SO42-等杂质,必须精制后才能供电解使用.氯碱厂电解饱和食盐水制取NaOH的工艺流程如下: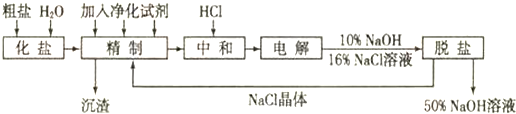
已知NaOH、NaCl在水中的溶解度数据如表:
(1)精制过程中会发生多种化学反应,写出其中一种反应的化学反应方程式Na2CO3+CaCl2=CaCO3↓+2NaCl.
(2)检验中和过程中碱性物质已反应完全的方法是取反应后的溶液少量加酚酞,溶液不显红色;
(3)脱盐过程中不需要的操作是c(填序号)
a.过滤 b.加热浓缩 c.冷却结晶 d.蒸发结晶
(4)上述工艺流程中可以循环使用的物质是NaCl(写化学式)

已知NaOH、NaCl在水中的溶解度数据如表:
| 温度0C | 20 | 30 | 40 | 50 | 60 | 70 | 80 | 90 | 100 |
| NaOH/g | 109 | 118 | 129 | 146 | 177 | 300 | 313 | 318 | 337 |
| NaCl/g | 36 | 36.3 | 36.6 | 37 | 37.3 | 37.8 | 38.4 | 39 | 39.8 |
(2)检验中和过程中碱性物质已反应完全的方法是取反应后的溶液少量加酚酞,溶液不显红色;
(3)脱盐过程中不需要的操作是c(填序号)
a.过滤 b.加热浓缩 c.冷却结晶 d.蒸发结晶
(4)上述工艺流程中可以循环使用的物质是NaCl(写化学式)
18.市监测站对空气质量进行在线自动监测,如表是我市清明节的空气质量日报
下列情况对表中三个空气质量指标不会产生影响的是( )
| 项目 | 空气污染指数 | 空气质量级别 | 空气质量 |
| 可吸入颗粒物 | 60 | Ⅱ | 良 |
| 二氧化硫 | 6 | ||
| 二氧化氮 | 20 |
| A. | 用煤做燃料 | B. | 露天焚烧垃圾 | C. | 生物的呼吸作用 | D. | 汽车排放尾气 |
15.下列说法中正确的是( )
| A. | 木炭点燃后生成黑色固体 | B. | 铁丝伸入氧气瓶中剧烈燃烧 | ||
| C. | 红磷在空气中不能燃烧 | D. | 硫点燃后产生有刺激性气味的气体 |
19.下列微粒结构示意图中,表示阳离子的是( )
| A. | 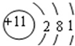 | B. | 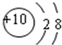 | C. | 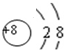 | D. |  |
2.硬水中含有较多可溶性钙、镁化合物,为降低水的硬度,下列方法可行的是( )
| A. | 煮沸 | B. | 静置 | C. | 过滤 | D. | 吸附 |