题目内容
11.将含有杂质的CaCO3 样品25g放入盛有100g稀盐酸的烧杯中,恰好完全反应,反应后称得剩余物质的质量为116.2g.(注:杂质不反应)请计算:(1)反应生成气体的质量为:8.8g.
(2)所用稀盐酸的质量分数.
分析 碳酸钙和稀盐酸反应生成氯化钙、水和二氧化碳,反应前后的质量差即为反应生成二氧化碳的质量,根据二氧化碳质量可以计算氯化氢的质量,进一步可以计算所用稀盐酸的质量分数.
解答 解:(1)反应生成气体的质量为:25g+100g-116.2g=8.8g.
故填:8.8.
(2)设稀盐酸中氯化氢质量为x,
CaCO3+2HCl═CaCl2+H2O+CO2↑,
73 44
x 8.8g
$\frac{73}{x}$=$\frac{44}{8.8g}$,
x=14.6g,
所用稀盐酸的质量分数为:$\frac{14.6g}{100g}$×100%=14.6%,
答:所用稀盐酸的质量分数为14.6%.
点评 差量法在计算中的应用很广泛,解答的关键是要分析出物质的质量差与要求的未知数之间的关系,再根据具体的数据求解.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
6.下列实验现象描述正确的是( )
| A. | 木炭在空气中燃烧产生蓝紫色火焰 | |
| B. | 稀硫酸中滴加酚酞试液,溶液变红 | |
| C. | 镁条在氧气中燃烧,生成黑色固体 | |
| D. | 鱼、虾能在水中生存说明水中溶有氧气 |
16.以往生产自来水使用适量的氯气,因为氯气可以和水反应得到HCl和HClO(次氯酸),HClO 能杀菌消毒.而新型净水剂高铁酸钠(Na2FeO4)的效果更好,且对人体无害.下列说法正确的是( )
| A. | 氯气的化学式为 Cl | |
| B. | HClO 杀菌消毒是化学变化 | |
| C. | 高铁酸钠是氧化物 | |
| D. | 用高铁酸钠净化生产的自来水是纯净物 |
20.小明同学对研究物质的酸碱性产生了浓厚的兴趣,他使用pH试纸测得家中某些物质近似的pH如表:
小明将自制的紫菜薹汁滴入上述7种物质中,发现紫菜薹汁与紫色石蕊试液的变化相似,将紫菜薹汁滴入肥皂液中,液体变成绿色.
(1)若将紫菜薹汁滴入护发素中,你认为液体的颜色变红色(填“不变”、“变红色”或“变绿色”)
(2)通过研究,小明同学懂得了洗发时先用洗发水再用护发素的科学道理.查阕资料:人体胃液pH在0.5~1.5之间,小明同学懂得了患胃酸过多的病人不能空腹食用上述食物中的苹果汁.
(3)要洗去学校餐厅地面上的油垢,小明同学准备从家中选择带a“洁厕灵”、b“厨房清洁剂”两种物质中的b(选“a”或“b”).
| 物质 | 洁厕灵 | 苹果汁 | 护发素 | 玉米粥 | 洗发水 | 肥皂液 | 厨房 洗洁剂 |
| PH | 1 | 3 | 6 | 7~8 | 8 | 10 | 12 |
(1)若将紫菜薹汁滴入护发素中,你认为液体的颜色变红色(填“不变”、“变红色”或“变绿色”)
(2)通过研究,小明同学懂得了洗发时先用洗发水再用护发素的科学道理.查阕资料:人体胃液pH在0.5~1.5之间,小明同学懂得了患胃酸过多的病人不能空腹食用上述食物中的苹果汁.
(3)要洗去学校餐厅地面上的油垢,小明同学准备从家中选择带a“洁厕灵”、b“厨房清洁剂”两种物质中的b(选“a”或“b”).
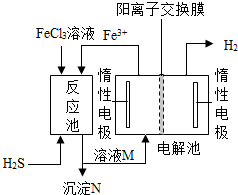 现代工业生产中常用电解氯化亚铁的方法制得氯化铁溶液,并用所得的氯化铁溶液吸收有毒的硫化氢气体.工艺原理如图所示.
现代工业生产中常用电解氯化亚铁的方法制得氯化铁溶液,并用所得的氯化铁溶液吸收有毒的硫化氢气体.工艺原理如图所示.