题目内容
盐酸和氢氧化钠溶液发生反应过程中溶液的pH变化如图一,请分析并回答问题: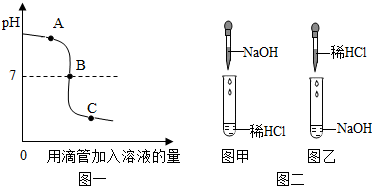
(1)根据pH变化图象判断,该反应的实验过程是按照图二中的图 (选填“甲”或“乙”)进行.
(2)图一中A、B、C三点表示的溶液,二种反应物恰好完全反应的是 (选填“A”“B”或“C”,下同)点的溶液:加入紫色石蕊溶液会呈现红色的是 点的溶液,此时溶液中一定含有的阳离子是 .
(3)为了探究盐酸与氢氧化钠溶液反应的生成物,小明的实验操作过程如下:
实验过程:向装有一定量稀盐酸的试管中滴加氢氧化钠溶液,振荡后再滴加硝酸银溶液.
得出结论:证明生成了氯化钠
小思认为该结论不正确,合理的解释是 .

(1)根据pH变化图象判断,该反应的实验过程是按照图二中的图
(2)图一中A、B、C三点表示的溶液,二种反应物恰好完全反应的是
(3)为了探究盐酸与氢氧化钠溶液反应的生成物,小明的实验操作过程如下:
实验过程:向装有一定量稀盐酸的试管中滴加氢氧化钠溶液,振荡后再滴加硝酸银溶液.
得出结论:证明生成了氯化钠
小思认为该结论不正确,合理的解释是
考点:中和反应及其应用,酸碱指示剂及其性质,溶液的酸碱性与pH值的关系
专题:常见的酸 酸的通性
分析:(1)根据溶液pH的变化趋势来分析;
(2)恰好完全中和,溶液呈中性;根据紫色石蕊试液的变色情况来分析;
(3)氯离子能与银离子结合成白色沉淀.
(2)恰好完全中和,溶液呈中性;根据紫色石蕊试液的变色情况来分析;
(3)氯离子能与银离子结合成白色沉淀.
解答:解:(1)由图示看出,溶液的pH是由大于7到等于7再到小于7,是由碱性到中性再到酸性,甲图是向酸中滴加碱溶液,乙图是向碱溶液中滴加酸,符合左图pH变化的应该是向碱溶液中加酸;故填:乙;
(2)盐酸和氢氧化钠完全中和时,溶液呈中性,pH=7,则是B点;酸性溶液能使紫色石蕊试液变红色,酸性溶液的pH小于7,酸性溶液中有氯化钠和HCl,故填:B;Na+和H+;
(3)不但氯化钠溶液能与硝酸银溶液反应产生氯化银白色沉淀,盐酸也能与硝酸银溶液反应产生氯化银白色沉淀,故填:稀盐酸也会与硝酸银反应生成白色的氯化银沉淀.
(2)盐酸和氢氧化钠完全中和时,溶液呈中性,pH=7,则是B点;酸性溶液能使紫色石蕊试液变红色,酸性溶液的pH小于7,酸性溶液中有氯化钠和HCl,故填:B;Na+和H+;
(3)不但氯化钠溶液能与硝酸银溶液反应产生氯化银白色沉淀,盐酸也能与硝酸银溶液反应产生氯化银白色沉淀,故填:稀盐酸也会与硝酸银反应生成白色的氯化银沉淀.
点评:本题是考查中和反应过程中溶液pH的变化情况的,我们要知道向酸中加碱和向碱中加酸时,溶液pH的变化趋向.明确不同指示剂的变色范围.

练习册系列答案
相关题目
如图为某反应的微观示意图,其中不同的球代表不同元素的原子.下列说法正确的是( )


| A、该反应为复分解反应 |
| B、生成物中有一种是氧化物 |
| C、乙中元素的化合价在反应前后保持不变 |
| D、反应前后分子的种类和数目都不变 |
 归纳总结是化学学习的常用方法,下图是对生成物质A的反应关系的归纳与整理.
归纳总结是化学学习的常用方法,下图是对生成物质A的反应关系的归纳与整理.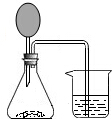 如图所示,老师为学生们准备了一套实验装置.通过实验现象判断物质反应的吸热、放热情况.小明向锥形瓶内的铝粉中滴加稀盐酸,发现烧杯中导管口出现气泡,于是得出结论:铝和稀盐酸反应放热,他的说法合理吗
如图所示,老师为学生们准备了一套实验装置.通过实验现象判断物质反应的吸热、放热情况.小明向锥形瓶内的铝粉中滴加稀盐酸,发现烧杯中导管口出现气泡,于是得出结论:铝和稀盐酸反应放热,他的说法合理吗 如图是A、B、C三种物质的溶解度曲线,根据下图回答下列问题:
如图是A、B、C三种物质的溶解度曲线,根据下图回答下列问题: 天宫一号是中国首个空间实验室,飞行器百余器件由哈尔滨制造,天宫一号目标飞行器的资源舱和实验舱铝合金材料多数产自东轻.主要利用铝合金的
天宫一号是中国首个空间实验室,飞行器百余器件由哈尔滨制造,天宫一号目标飞行器的资源舱和实验舱铝合金材料多数产自东轻.主要利用铝合金的