题目内容
12.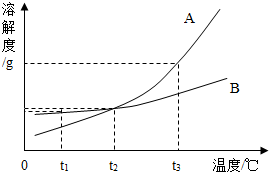 如图是A,B两种溶质的溶解度曲线,下列说法不正确的是( )
如图是A,B两种溶质的溶解度曲线,下列说法不正确的是( )| A. | t1时,A的某种溶液的溶质质量分数一定比B的某种溶液的溶质质量分数小 | |
| B. | t2时,A,B两种溶质的溶解度相等 | |
| C. | 将t2的A,B两种溶质的饱和溶液各100g降温至t1析出晶体质量的关系是A>B | |
| D. | 可以通过降温或者蒸发溶剂的方法使他们的不饱和溶液变成饱和溶液 |
分析 A、根据不知道A、B溶液是否饱和,所以无法比较二者的溶质质量分数的大小进行解答;
B、根据溶解度曲线可知,t2时,A,B两种溶质的溶解度相等进行解答;
C、根据溶解度曲线可知,A的溶解度受温度的影响比B大进行解答;
D、根据A、B溶解度随温度的降低而减小进行解答.
解答 解:A、不知道A、B溶液是否饱和,所以无法比较二者的溶质质量分数的大小,所以不能判断t1时,A的某种溶液的溶质质量分数一定比B的某种溶液的溶质质量分数小,故A错误;
B、根据溶解度曲线可知,t2时,A,B两种溶质的溶解度相等,故B正确;
C、根据溶解度曲线可知,A的溶解度受温度的影响比B大,所以将t2的A,B两种溶质的饱和溶液各100g降温至t1析出晶体质量的关系是A>B,故C正确;
D、A、B溶解度随温度的降低而减小,所以通过降温或者蒸发溶剂的方法使他们的不饱和溶液变成饱和溶液,故D正确.
故选:A.
点评 利用溶解度曲线图可以判断在不同的温度下同一固体物质溶解度受温度的影响情况,也可以判断不同物质在同一温度下的大小情况.

练习册系列答案
相关题目
11.下列除杂质的试剂和方法不正确的是( )
| 选项 | 物质(括号内为杂质) | 除杂方法 |
| A | Cu(CuO) | 加入足量稀硫酸,洗涤,干燥 |
| B | KCl(MnO2) | 溶解、过滤、蒸发结晶 |
| C | CO2(水蒸气) | 通过盛有烧碱固体的干燥管 |
| D | CaO(CaCO3) | 高温煅烧 |
| A. | A | B. | B | C. | C | D. | D |
7.如图为物质的分类关系,①与②是并列关系,③包含在②中,下列说法错误的是( )
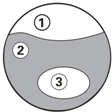

| A. | 若①是单质,则②可以是化合物,③可能是氧化物 | |
| B. | ①如果是空气,则②可以是钢 | |
| C. | 若①是有机物,则③可以是碳酸钙 | |
| D. | 若②化合物,则③可以是碱 |
17.如图是物质A、B、C的溶解度曲线,下列相关说法正确的是( )
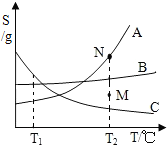

| A. | 若要将B从溶液中结晶出来常采用的方法是降温结晶 | |
| B. | 将T2℃时A、B、C的饱和溶液冷却到T1℃,A溶液的溶质质量分数最小 | |
| C. | 若要将组成在M点的A溶液转变为N点的溶液,只能采取恒温蒸发溶剂的方法 | |
| D. | 将T2℃时组成在M点的C与水的混合物降温至T1℃时,可能得到C的不饱和溶液 |
4. 某化学兴趣小组的同学为了探究“复分解反应发生的条件”,做了两个实验:
某化学兴趣小组的同学为了探究“复分解反应发生的条件”,做了两个实验:
①CuSO4溶液与NaOH溶液、②CuSO4溶液与BaCl2溶液反应.实验结束后将两次实验中的废液倒入同一个干净的烧杯中,充分混合后过滤,得到滤液呈无色.
(1)写出实验②发生反应的化学方程式:CuSO4+BaCl2=BaSO4↓+CuCl2.
(2)取少量滤液于试管中,滴入紫色石蕊试液,石蕊溶液为紫色,则滤液呈中性(填“酸”、“中”、“碱”). 废液在烧杯中混合后,肯定发生的化学反应的方程式:CuCl2+2NaOH=Cu(OH)2↓+2NaCl.
(3)该小组的同学对滤液中溶质的成分继续进行了如下探究实验:
【提出问题】滤液中溶质的成分是什么?
【作出猜想】小红认为:只含氯化钠;
小明认为:可能含有硫酸钠、氯化钠和氯化钡;
小亮认为:可能含氯化钠和氯化钡;
你认为:还可能是氯化钠和硫酸钠(写一种猜想).
【讨论】你认为小红、小明、小亮三位同学中谁的猜想明显不合理?为什么?小明;因为氯化钡与硫酸钠反应生成沉淀,不能在溶液中共存
【实验探究】
【交流拓展】a.要使蓝色溶液变成无色,除了加入NaOH等碱性溶液外,还可以在蓝色溶液中加入足量的Mg或Al或Zn.
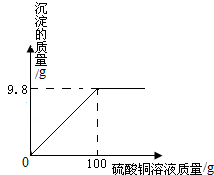
b.在盛有100g氢氧化钠溶液的大烧杯中缓缓加入硫酸铜溶液,反应生成沉淀的质量与加入硫酸铜溶液质量的关系如图所示:求恰好完全反应时,所得溶液中溶质的质量分数?(精确到0.1% )
 某化学兴趣小组的同学为了探究“复分解反应发生的条件”,做了两个实验:
某化学兴趣小组的同学为了探究“复分解反应发生的条件”,做了两个实验:①CuSO4溶液与NaOH溶液、②CuSO4溶液与BaCl2溶液反应.实验结束后将两次实验中的废液倒入同一个干净的烧杯中,充分混合后过滤,得到滤液呈无色.
(1)写出实验②发生反应的化学方程式:CuSO4+BaCl2=BaSO4↓+CuCl2.
(2)取少量滤液于试管中,滴入紫色石蕊试液,石蕊溶液为紫色,则滤液呈中性(填“酸”、“中”、“碱”). 废液在烧杯中混合后,肯定发生的化学反应的方程式:CuCl2+2NaOH=Cu(OH)2↓+2NaCl.
(3)该小组的同学对滤液中溶质的成分继续进行了如下探究实验:
【提出问题】滤液中溶质的成分是什么?
【作出猜想】小红认为:只含氯化钠;
小明认为:可能含有硫酸钠、氯化钠和氯化钡;
小亮认为:可能含氯化钠和氯化钡;
你认为:还可能是氯化钠和硫酸钠(写一种猜想).
【讨论】你认为小红、小明、小亮三位同学中谁的猜想明显不合理?为什么?小明;因为氯化钡与硫酸钠反应生成沉淀,不能在溶液中共存
【实验探究】
| 实验操作 | 实验现象 | 实验结论 |
| 实验A:取少量滤液于试管中,加入 适量纯碱溶液,振荡. | 无明显现象 | 滤液中不含BaCl2 |
| 实验B:取少量滤液于试管中,加入适量硝酸钡溶液,振荡. | 产生白色沉淀 | 滤液中含有Na2SO4 |
b.在盛有100g氢氧化钠溶液的大烧杯中缓缓加入硫酸铜溶液,反应生成沉淀的质量与加入硫酸铜溶液质量的关系如图所示:求恰好完全反应时,所得溶液中溶质的质量分数?(精确到0.1% )
1.实验操作有误或不规范,很可能造成实验失败甚至酿成事故,下列实验操作正确的是( )
| A. | 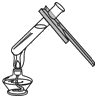 给液体加热 | B. | 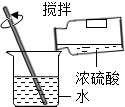 稀释浓硫酸 | ||
| C. | 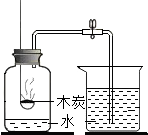 测定空气里氧气含量 | D. |  称量氢氧化钠 |
2.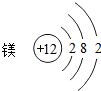 依据如图的原子结构示意图,下列说法正确的是( )
依据如图的原子结构示意图,下列说法正确的是( )
 依据如图的原子结构示意图,下列说法正确的是( )
依据如图的原子结构示意图,下列说法正确的是( )| A. | 该原子的核电荷数为12 | B. | 该原子核外有两个电子 | ||
| C. | 该原子在反应中易得到电子 | D. | 该原子在反应中容易成为阴离子 |