题目内容
18.“毒胶囊”泛指利用由工业皮革废料为原料生产的含重金属铬(Cr)超标的胶囊,其中含有可能引起人体肾伤害的+6 价的铬.下列铬的化合物中铬呈+6 价的是( )| A. | Cr2(SO4)3 | B. | Cr2O3 | C. | K2Cr2O7 | D. | Cr(OH)3 |
分析 根据在化合物中正负化合价代数和为零,结合选项中铬的化合物的化学式进行解答即可.
解答 解:A、硫酸根显-2价,设Cr2(SO4)3中铬元素的化合价是x,根据在化合物中正负化合价代数和为零,可得:2x+(-2)×3=0,则x=+3价.
B、氧元素显-2价,设Cr2O3中氯元素的化合价是y,根据在化合物中正负化合价代数和为零,可得:2y+(-2)×3=0,则y=+3价.
C、钾元素显+1价,氧元素显-2价,设K2CrO7中铬元素的化合价是z,根据在化合物中正负化合价代数和为零,可得:(+1)×2+z+(-2)×4=0,则z=+6价.
D、氢氧根显-1价,设Cr(OH)3中铬元素的化合价是w,根据在化合物中正负化合价代数和为零,可得:w+(-1)×3=0,则w=+3价.
故铬的化合物中铬呈+6价的是K2CrO7.
故选:C.
点评 本题难度不大,掌握利用化合价的原则(化合物中正负化合价代数和为零)计算指定元素的化合价的方法即可正确解答此类题.

练习册系列答案
相关题目
8.20世纪20年代,丹麦和英国的一些化学家提出了新的酸碱理论--“质子论”.质子论认为:凡能放出质子(即H+)的分子或离子都是酸,凡能结合质子的分子或离子都是碱.根据这个理论,下列说法正确的是( )
| A. | H2SO4属于酸 | B. | CO32-属于酸 | C. | NO3-属于碱 | D. | Na+属于碱 |
6.小黎同学为了进一步加深对“碱的化学性质”的理解,特邀你协助完成下列活动与探究:
(1)如图1所示,在白色点滴板上进行实验,请将实验现象填入下表:
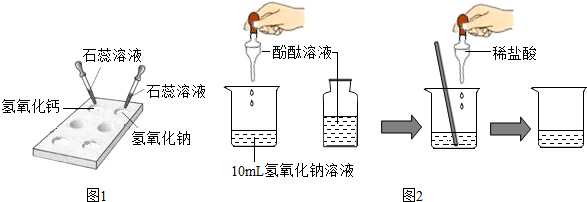
(2)回忆检验二氧化碳气体的反应,写出该反应的化学方程式CO2+Ca(OH)2═CaCO3↓+H2O.
(3)二氧化硫(SO2)与氢氧化钠反应与上面的反应类似,写出这一反应的化学方程式SO2+2NaOH═Na2SO3+H2O.
(4)如图2所示,在烧杯中加入10mL氢氧化钠溶液,滴入几滴酚酞试液,溶液显红色,再用滴管慢慢滴入稀盐酸,并不断搅拌溶液,至溶液颜色恰好变成无色为止,说明溶液呈中性.写出该反应的化学方程式NaOH+HCl═NaCl+H2O反应类型复分解反应;由此可知:中和反应的实质是H+和OH-反应生成H2O.
(5)根据上面的实验和讨论,试归纳出氢氧化钠、氢氧化钙有哪些相似的化学性质.(任写两点)
①都能使酸碱指示剂变色;
②碱能与酸性氧化物反应生成盐和水.
(1)如图1所示,在白色点滴板上进行实验,请将实验现象填入下表:
| 氢氧化钠溶液 | 氢氧化钙溶液 | |
| 加紫色石蕊溶液 | 蓝色 | 蓝色 |

(2)回忆检验二氧化碳气体的反应,写出该反应的化学方程式CO2+Ca(OH)2═CaCO3↓+H2O.
(3)二氧化硫(SO2)与氢氧化钠反应与上面的反应类似,写出这一反应的化学方程式SO2+2NaOH═Na2SO3+H2O.
(4)如图2所示,在烧杯中加入10mL氢氧化钠溶液,滴入几滴酚酞试液,溶液显红色,再用滴管慢慢滴入稀盐酸,并不断搅拌溶液,至溶液颜色恰好变成无色为止,说明溶液呈中性.写出该反应的化学方程式NaOH+HCl═NaCl+H2O反应类型复分解反应;由此可知:中和反应的实质是H+和OH-反应生成H2O.
(5)根据上面的实验和讨论,试归纳出氢氧化钠、氢氧化钙有哪些相似的化学性质.(任写两点)
①都能使酸碱指示剂变色;
②碱能与酸性氧化物反应生成盐和水.
13.下列物质的用途,与该物质的化学性质有关的是( )
| A. | 用氢气填充探空气球 | B. | 用金刚石切割玻璃 | ||
| C. | 用干冰进行人工降雨 | D. | 用盐酸除去铁锈 |
3.分类是学习和研究化学物质及其变化的一种常用的基本方法.现有生铁,它与下列哪组属于同一类物质( )
| A. | 硫酸亚铁、氯化铁 | B. | 不锈钢、空气 | ||
| C. | 氧化铁、四氧化三铁 | D. | 铁粉、锌粉 |
8.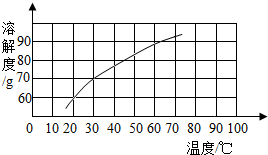 木糖醇是一种理想的蔗糖替代品,它的溶解度曲线如图所示.下列关于木糖醇的叙述正确的是( )
木糖醇是一种理想的蔗糖替代品,它的溶解度曲线如图所示.下列关于木糖醇的叙述正确的是( )
 木糖醇是一种理想的蔗糖替代品,它的溶解度曲线如图所示.下列关于木糖醇的叙述正确的是( )
木糖醇是一种理想的蔗糖替代品,它的溶解度曲线如图所示.下列关于木糖醇的叙述正确的是( )| A. | 木糖醇的溶解度随温度的升高而降低 | |
| B. | 30℃时,木精醇的溶解度是70g | |
| C. | 50℃时,100 g水中加入80 g木糖醇,搅拌,可得到饱和溶液 | |
| D. | 70℃时木糖醇的饱和溶液降温到60℃不会析出木糖醇晶体 |
 人通过肺与外界进行气体交换,消耗空气中的部分氧气,排出二氧化碳、水蒸气等气体.但人体排出的二氧化碳究竟是吸入空气中原有的,还是人体代谢的最终产物?为了证实这个问题,有人采用以下装置进行实验(如图).
人通过肺与外界进行气体交换,消耗空气中的部分氧气,排出二氧化碳、水蒸气等气体.但人体排出的二氧化碳究竟是吸入空气中原有的,还是人体代谢的最终产物?为了证实这个问题,有人采用以下装置进行实验(如图).