题目内容
1.为了检验氢氧化钠溶液是否变质,可取少量样品,向溶液中加入盐酸,经检验氢氧化钠溶液部分已变质.除去氢氧化钠溶液中的杂质(变质成分)的化学方程式为Na2CO3+Ca(OH)2═CaCO3↓+2NaOH.分析 物质在存放时要防止变质,变质的原因可能与空气中的某种成分发生化学反应,比如氢氧化钠、氢氧化钙等碱性物质能与空气中的二氧化碳发生化学反应生成碳酸盐,而导致化学试剂失效.因此检验方法可以从如何检验碳酸根离子出发.对于杂质的去除可以在不引入其它离子的同时,将碳酸根离子生成沉淀,过滤去掉.
解答 解:氢氧化钠溶液能够吸收空气中的二氧化碳,氢氧化钠和二氧化碳反应能生成碳酸钠和水,稀盐酸能和碳酸盐反应生成二氧化碳气体,可以向氢氧化钠溶液中加入稀盐酸来检验氢氧化钠溶液是否变质.故填:盐酸.
如果氢氧化钠变质了,那么溶液中存在着碳酸钠,可以向溶液中加入适量的氢氧化钡溶液或氢氧化钙溶液把碳酸钠除去,并且不带入新杂质,碳酸钠和氢氧化钡、氢氧化钙反应的化学方程式分别为:Na2CO3+Ba(OH)2═BaCO3↓+2NaOH,Na2CO3+Ca(OH)2═CaCO3↓+2NaOH.
故填:Na2CO3+Ba(OH)2═BaCO3↓+2NaOH或Na2CO3+Ca(OH)2═CaCO3↓+2NaOH
点评 本题综合考查了氢氧化钠的性质以及碳酸根的检验方法及除杂方法,注意把握加入试剂的量,除杂过程中不能加入新的杂质离子,正确选择试剂.

练习册系列答案
 考前必练系列答案
考前必练系列答案
相关题目
11.钛和钛合金被认为是21世纪最重要的金属材料,它具有熔点高、密度小、抗腐蚀性强等优良性能,广泛应用于军事、船泊、化工等.已知钛原子的质子数是22,中子数是24,则钛原子的核外电子数、相对原子质量分别是( )
| A. | 22 46 | B. | 22 24 | C. | 24 22 | D. | 24 46 |
12.物质与水发生的复分解反应称为水解反应,如:Al2S3+6H2O=2Al(OH)3↓+3H2S↑.下列反应中,不属于水解反应的是( )
| A. | NaF+H2O═NaOH+HF | B. | C+H2O(气态)$\frac{\underline{\;高温\;}}{\;}$CO+H2 | ||
| C. | Mg3N2+6H2O═3Mg(OH)2↓+2NH3↑ | D. | CaO2+2H2O═Ca(OH)2+H2O2 |
6.下列实验操作中,不正确的是( )
| A. | 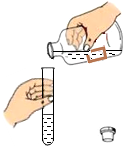 倾倒液体 | B. | 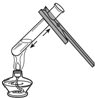 加热液体 | C. | 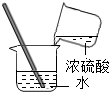 稀释浓硫酸 稀释浓硫酸 | D. | 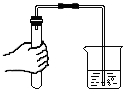 检查气密性 |
13.工业上用甲、乙制备化学肥料丙,同时生成丁.根据下图得出的结论中,不正确的是( )
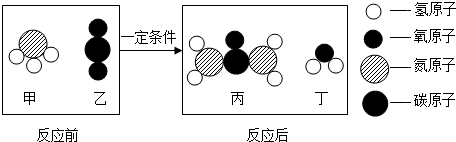

| A. | 甲的化学式为NH3 | B. | 乙和丁属于氧化物 | ||
| C. | 丙中氮元素质量分数约为23.3% | D. | 反应中的甲和乙分子个数比为2:1 |
10.下列物质所对应用途不正确的是( )
| A. | 氧化钙:作干燥剂 | B. | 氢氧化钠:治疗胃酸过多 | ||
| C. | 干冰:作制冷剂 | D. | 氧气:供给呼吸 |
11.高铁酸钠(Na2FeO4)是一种新型高效的水处理剂,下列有关高铁酸钠的说法正确的是( )
| A. | 铁元素化合价为+6 | B. | 钠、铁、氧三种元素质量比是2:1:4 | ||
| C. | 属于氧化物 | D. | 由两种金属和一种非金属组成 |