题目内容
8.2015年10月,我国科学家屠呦呦由于发现了青蒿素(C15H22O5)而获得诺贝尔医学奖.下列有关青蒿素的说法不正确的是( )| A. | 青蒿素是一种有机物 | B. | 青蒿素中碳、氢原子个数比为15:22 | ||
| C. | 青蒿素由三种元素组成 | D. | 青蒿素的相对分子质量为42 |
分析 A.根据有机物的概念来分析;
B.根据分子结构来分析;
C.根据化学式的意义考虑;
D.根据相对分子质量的计算方法来分析
解答 解;A.青蒿素是一种由碳元素组成的化合物,故属于有机物,故正确;
B.由青篙素的化学式C15H22O5可知,碳、氢原子个数比为:15:22,故正确;
C.由青篙素的化学式C15H22O5可知,青篙素由碳、氢、氧三种元素组成,故正确;
D.相对分子质量是构成分子的所有原子的相对原子质量之和,可表示为:12×15+1×22+16×5═282,故错误.
故选D
点评 本题难度不大,考查同学们结合新信息、灵活运用化学式的含义与有关计算进行分析问题、解决问题的能力.

练习册系列答案
 字词句段篇系列答案
字词句段篇系列答案
相关题目
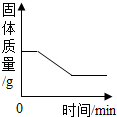
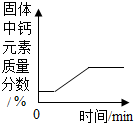
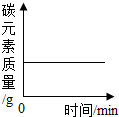
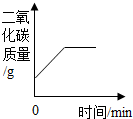
11.某露置于空气中的生石灰干燥剂,测得其中Ca元素质量分数为60%,向10g干燥剂中加足量稀盐酸使其完全溶解.正确的说法是( )
| A. | 加入盐酸一定有气泡产生 | |
| B. | 生成CaCl2的物质的量为0.15mol | |
| C. | 此包干燥剂的组成可能是CaCO3 | |
| D. | 干燥剂的成分可能是Ca(OH)2、CaCO3的混合物 |
3.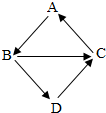 如图中A、B、C、D均为初中阶段常见物质,它们转化关系用如图所示.下列说法中错误的是( )
如图中A、B、C、D均为初中阶段常见物质,它们转化关系用如图所示.下列说法中错误的是( )
 如图中A、B、C、D均为初中阶段常见物质,它们转化关系用如图所示.下列说法中错误的是( )
如图中A、B、C、D均为初中阶段常见物质,它们转化关系用如图所示.下列说法中错误的是( )| A. | 若A、C、D均为白色固体,则B→D的反应可能是中和反应 | |
| B. | 若B为红色固体单质,则D可能为绿色固体 | |
| C. | 若B、C、D为气体,则A可能为常见的液体 | |
| D. | 若C、D为元素组成相同的氧化物,则A可能为氧气 |
20.氢氧化钠是一种重要的化工原料,也是实验室中常见的一种试剂,氢氧化钠必须密封保存,用化学方程式表示变质原因2NaOH+CO2═Na2CO3+H2O.
探究一:确定一瓶氢氧化钠固体是否变质
探究二:确定氢氧化钠固体变质的程度
实验方案中滴入过量的CaCl2溶液目的是除尽碳酸钠.
探究一:确定一瓶氢氧化钠固体是否变质
| 实验操作 | 实验现象 | 结论 |
| 取少量样品于试管中,加入适量水,样品全溶解后,滴加足量的稀盐酸(填一种溶液名称) | 有气泡产生 | 氢氧化钠固体已变质 |
| 实验操作 | 实验现象 | 结论 |
| ①取少量样品于试管中,加入适量水,样品全溶解后,滴加过量的CaCl2溶液 | 产生白色沉淀 | 氢氧化钠固体部分变质 |
| ②静置后取上层清液于试管中,滴入2滴酚酞试液 | 溶液变为红色 |
17.PM2.5是指大气中直径不超过2.5μm的颗粒物,主要来源是化石燃料的燃烧和扬尘.它是造成雾霾天气的元凶之一,吸入人体后能直接进入支气管,因而对人体健康影响更大.下列措施能减少PM2.5污染的是( )
| A. | 鼓励焚烧秸秆节约能源 | B. | 鼓励燃煤火力发电 | ||
| C. | 鼓励使用太阳能热水器 | D. | 鼓励开私家车出行 |
18. 某学习小组探究氢氧化钙溶液的化学性质,并作了延伸探究.
某学习小组探究氢氧化钙溶液的化学性质,并作了延伸探究.
探究一:甲同学设计了如下实验方案,请你帮助完成实验报告.
探究一:甲同学设计了如下实验方案,请你帮助完成实验报告.
【提出问题】实验方案(3)褪色后溶液中的溶质是什么?
【查阅资料】氯化钙溶液呈中性.
【作出猜想】乙同学从反应情况分析,溶液中除含少量酚酞外,溶质可能有以下三种情况:
①氯化钙;②氯化钙和氯化氢;③氯化钙和氢氧化钙
【分析讨论】丙同学从实验现象分析得出:猜想③肯定不合理,其理由是稀盐酸加入滴有酚酞的石灰水中,红色褪为无色,说明溶液为中性或酸性,不可能有氢氧化钙,故猜想③肯定不合理;.
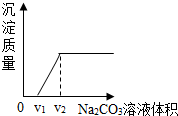
探究二:丁同学为进一步验证乙同学的猜想,设计实验如下:将实验方案(3)褪色后溶液倒入烧杯中,向其中逐滴滴加稀碳酸钠溶液至过量,边滴边振荡.实验后得出产生沉淀质量与滴加碳酸钠溶液体积之间的关系,如图所示.写出实验过程中的现象滴加碳酸钠溶液,开始先产生气泡,随后才产生沉淀,溶液最终变红色.
【得出结论】乙同学的猜想中,②(填序号)合理.
【反思讨论】学习小组结合图象,分析了丁同学实验过程中烧杯内溶液的变化.下列说法正确的是AB.(填序号)
A.溶液质量逐渐增大 B.氯化钠质量逐渐增大,V2后不变
C.氯化钙的质量先增大后减小 D.溶液的pH一直在增大.
 某学习小组探究氢氧化钙溶液的化学性质,并作了延伸探究.
某学习小组探究氢氧化钙溶液的化学性质,并作了延伸探究.探究一:甲同学设计了如下实验方案,请你帮助完成实验报告.
探究一:甲同学设计了如下实验方案,请你帮助完成实验报告.
| 方案 | (1) | (2) | (3) |
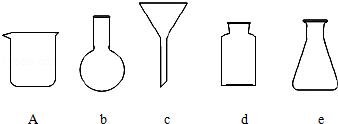
| 实验操作 | 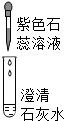 | 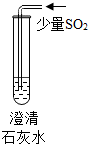 |  |
| 现象 | 溶液变为蓝色 | 澄清石灰水变浑浊 | 红色褪为无色 |
| 结论或解释 | 氢氧化钙溶液能使石蕊等酸碱指示剂变色 | 氢氧化钙溶液能与某些非金属氧化物反应生成盐和水.二氧化硫与澄清石灰水反应的化学方程式是 SO2+Ca(OH)2═CaSO3↓+H2O | 氢氧化钙溶液能与酸发生中和反应 |
【查阅资料】氯化钙溶液呈中性.
【作出猜想】乙同学从反应情况分析,溶液中除含少量酚酞外,溶质可能有以下三种情况:
①氯化钙;②氯化钙和氯化氢;③氯化钙和氢氧化钙
【分析讨论】丙同学从实验现象分析得出:猜想③肯定不合理,其理由是稀盐酸加入滴有酚酞的石灰水中,红色褪为无色,说明溶液为中性或酸性,不可能有氢氧化钙,故猜想③肯定不合理;.
探究二:丁同学为进一步验证乙同学的猜想,设计实验如下:将实验方案(3)褪色后溶液倒入烧杯中,向其中逐滴滴加稀碳酸钠溶液至过量,边滴边振荡.实验后得出产生沉淀质量与滴加碳酸钠溶液体积之间的关系,如图所示.写出实验过程中的现象滴加碳酸钠溶液,开始先产生气泡,随后才产生沉淀,溶液最终变红色.
【得出结论】乙同学的猜想中,②(填序号)合理.
【反思讨论】学习小组结合图象,分析了丁同学实验过程中烧杯内溶液的变化.下列说法正确的是AB.(填序号)
A.溶液质量逐渐增大 B.氯化钠质量逐渐增大,V2后不变
C.氯化钙的质量先增大后减小 D.溶液的pH一直在增大.