题目内容
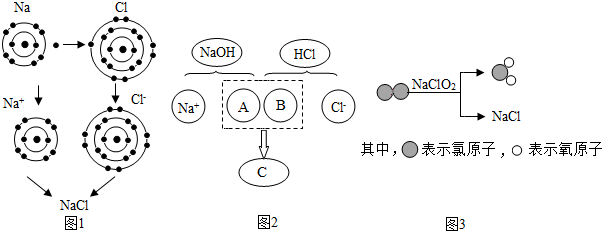
10.某校化学兴趣小组对一瓶溶液进行分析,初步确定它是含有同种阴离子的M、N混合液,继续分析的步骤如下(每一步骤都充分反应):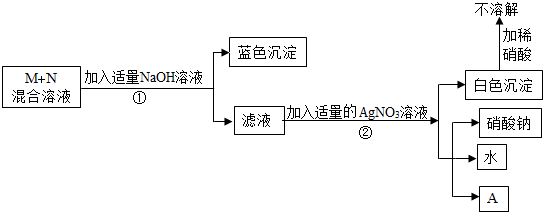
请根据过程及现象回答下列问题:
(1)若没有产物A,则M、N可能是NaCl和CuCl2(填化学式);步骤①中发生反应的化学方程式是CuCl2+2NaOH═Cu(OH)2↓+2NaCl;滤液中的溶质是NaCl(填化学式).
(2)若有产物A,且A是一种常见的复合肥,则M可能是KCl(填化学式).
分析 (1)根据滤液和硝酸银反应会生成不溶于硝酸的白色沉淀和硝酸钠,依据复分解反应原理可知,滤液中含有氯化钠,混合液中加氢氧化钠会生成蓝色沉淀,说明混合液中存在铜离子,M、N含有同种阴离子的M、N混合液,所以可能是氯化钠和氯化铜,然后将推出的物质代入转换关系中验证即可;
(2)根据产物A是一种复合钾肥,滤液和硝酸银反应会生成不溶于硝酸的白色沉淀和硝酸钠,依据复分解反应原理可知,滤液中含有氯化钠,混合液中加氢氧化钠会生成蓝色沉淀,说明混合液中存在铜离子,M、N含有同种阴离子的M、N混合液,但是钠离子会进入滤液中,所以M和N中存在钾离子,所以混合物可能是氯化钾和氯化铜,将推出的物质进行验证即可.
解答 解:(1)滤液和硝酸银反应会生成不溶于硝酸的白色沉淀和硝酸钠,混合液中加氢氧化钠会生成蓝色沉淀,说明混合液中存在铜离子,M、N含有同种阴离子的M、N混合液,所以可能是氯化钠和氯化铜,氯化铜和氢氧化钠反应生成氯化钠和氢氧化铜沉淀,化学方程式为:CuCl2+2NaOH═Cu(OH)2↓+2NaCl,依据复分解反应原理可知,滤液中含有氯化钠;
(2)产物A是一种复合钾肥,滤液和硝酸银反应会生成不溶于硝酸的白色沉淀和硝酸钠,依据复分解反应原理可知,滤液中含有氯化钠和氯化钾,混合液中加氢氧化钠会生成蓝色沉淀,说明混合液中存在铜离子,M、N含有同种阴离子的M、N混合液,但是钠离子会进入滤液中,所以M和N中存在钾离子,所以混合物可能是氯化钾和氯化铜.
故答案为:(1)NaCl,CuCl2,CuCl2+2NaOH═Cu(OH)2↓+2NaCl,NaCl;
(2)KCl.
点评 在解此类题时,首先将题中有特征的物质推出,然后结合推出的物质题中的转换关系推导剩余的物质,最后进行验证即可.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
15.实验室用溶质质量分数为6%的氯化钠溶液配制50g溶质质量分数为3%的氯化钠溶液.下列说法正确的是( )
| A. | 实验中不需使用玻璃棒搅拌 | |
| B. | 实验步骤是:计算、称取、量取、溶解、转移 | |
| C. | 量取水时,用规格为50mL的量筒量取所需蒸馏水 | |
| D. | 把配制好的氯化钠溶液倒入刚用蒸馏水润洗过的试剂瓶中,并贴上标签 |
7.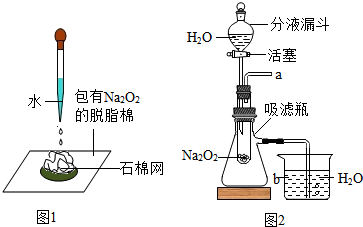 化学活动课上,老师表演了一个“水能生火”的魔术(如图1所示),他将包有过氧化钠(Na2O2)粉末的脱脂棉放在石棉网上,向脱脂棉上滴了几滴水,脱脂棉立刻燃烧起来,小红和小明也按图1所示操作,结果小红的魔术取得了成功,而小明没有看到有火生起,小明打开脱脂棉,发现脱脂棉上有白色固体,他们对比此展开了探究:
化学活动课上,老师表演了一个“水能生火”的魔术(如图1所示),他将包有过氧化钠(Na2O2)粉末的脱脂棉放在石棉网上,向脱脂棉上滴了几滴水,脱脂棉立刻燃烧起来,小红和小明也按图1所示操作,结果小红的魔术取得了成功,而小明没有看到有火生起,小明打开脱脂棉,发现脱脂棉上有白色固体,他们对比此展开了探究:
【查阅资料】Na2o3为淡黄色固体,能与水和二氧化碳反应.
【提出问题】水和过氧化钠作用能“生火”的原因是什么,脱脂棉上的白色固体成分是什么?
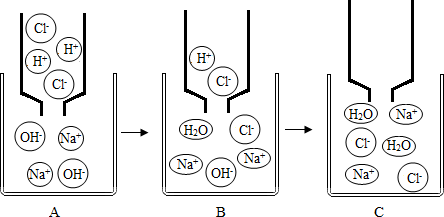
实验探究一;小红和小明在老师的指导下,设计了如图2所示装置进行探究实验,转动活塞,使水逐滴滴下,然后将带火星的木条放在a处,带火星的木条复燃,说明水和过氧化钠反应有氧气生成,伸入b中的导管口有气泡冒出,说明水和过氧化钠反应放出(填“吸收”或“放出”)热量.
实验探究二:(1)针对脱脂棉上的白色固体的成分是什么,小明提出三种猜想:
猜想1:白色固体是碳酸钠;
猜想2:白色固体都是氢氧化钠;
猜想3:白色固体是碳酸钠和氢氧化钠的混合物
为了验证猜想,小明设计了如下实验
(2)根据上述小明的实验结果,请写出Na2O2与水反应的化学方程式2Na2O2+2H2O=4NaOH+O2↑.
【实验拓展】请你分析小明魔术失败可能是什么原因引起的?提出你的猜想,并设计实验进行验证.
【提出猜想】滴加的水快且多
【设计实验】实验步骤:按图1所示操作分别进行,一个滴加水时快且多,一个滴加水时慢且少;
实验现象:滴加水时快且多的脱脂棉没有燃烧,滴加水时慢且少的脱脂棉燃烧起来;
实验结论:滴加水时快且多,温度不能达到脱脂棉的着火点,因此不能燃烧.
 化学活动课上,老师表演了一个“水能生火”的魔术(如图1所示),他将包有过氧化钠(Na2O2)粉末的脱脂棉放在石棉网上,向脱脂棉上滴了几滴水,脱脂棉立刻燃烧起来,小红和小明也按图1所示操作,结果小红的魔术取得了成功,而小明没有看到有火生起,小明打开脱脂棉,发现脱脂棉上有白色固体,他们对比此展开了探究:
化学活动课上,老师表演了一个“水能生火”的魔术(如图1所示),他将包有过氧化钠(Na2O2)粉末的脱脂棉放在石棉网上,向脱脂棉上滴了几滴水,脱脂棉立刻燃烧起来,小红和小明也按图1所示操作,结果小红的魔术取得了成功,而小明没有看到有火生起,小明打开脱脂棉,发现脱脂棉上有白色固体,他们对比此展开了探究:【查阅资料】Na2o3为淡黄色固体,能与水和二氧化碳反应.
【提出问题】水和过氧化钠作用能“生火”的原因是什么,脱脂棉上的白色固体成分是什么?
实验探究一;小红和小明在老师的指导下,设计了如图2所示装置进行探究实验,转动活塞,使水逐滴滴下,然后将带火星的木条放在a处,带火星的木条复燃,说明水和过氧化钠反应有氧气生成,伸入b中的导管口有气泡冒出,说明水和过氧化钠反应放出(填“吸收”或“放出”)热量.
实验探究二:(1)针对脱脂棉上的白色固体的成分是什么,小明提出三种猜想:
猜想1:白色固体是碳酸钠;
猜想2:白色固体都是氢氧化钠;
猜想3:白色固体是碳酸钠和氢氧化钠的混合物
为了验证猜想,小明设计了如下实验
| 实验步骤 | 实验现象 | 实验结论 |
| ①将脱脂棉上的固体取下,加水溶解,然后向其中加入足量的氯化钙溶液 | 无白色沉淀生成 | 白色固体中无硫酸钠 |
| ②取步骤①的溶液加入酚酞溶液 | 酚酞溶液变红色 | 猜想2成立 |
【实验拓展】请你分析小明魔术失败可能是什么原因引起的?提出你的猜想,并设计实验进行验证.
【提出猜想】滴加的水快且多
【设计实验】实验步骤:按图1所示操作分别进行,一个滴加水时快且多,一个滴加水时慢且少;
实验现象:滴加水时快且多的脱脂棉没有燃烧,滴加水时慢且少的脱脂棉燃烧起来;
实验结论:滴加水时快且多,温度不能达到脱脂棉的着火点,因此不能燃烧.
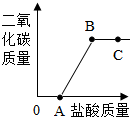 取实验室中某久置的氢氧化溶液,向其中滴加稀盐酸,绘制出生成的CO2的质量与加入的稀盐酸的质量关系如图所示,下列有关说法正确的是C.
取实验室中某久置的氢氧化溶液,向其中滴加稀盐酸,绘制出生成的CO2的质量与加入的稀盐酸的质量关系如图所示,下列有关说法正确的是C.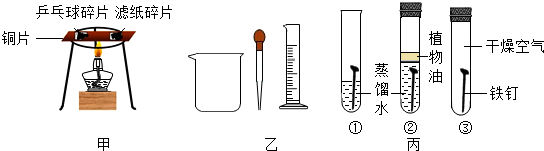
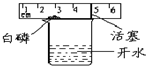 某同学用右图装置粗略测定空气中氧气的体积分数,图中烧杯上方玻璃管(预先固定好)中部有一可左右活动的活塞,活塞左端的玻璃管内密封有空气,活塞右端的玻璃管口跟空气连通,实验开始前活塞处在刻度5cm处.
某同学用右图装置粗略测定空气中氧气的体积分数,图中烧杯上方玻璃管(预先固定好)中部有一可左右活动的活塞,活塞左端的玻璃管内密封有空气,活塞右端的玻璃管口跟空气连通,实验开始前活塞处在刻度5cm处.