题目内容
5. 有一份铁粉与铜粉的混合物样品,为了解其组成,某同学用20克样品加入足量的稀硫酸中,待反应完全后过滤,称得不溶物质量为6克.试计算:
有一份铁粉与铜粉的混合物样品,为了解其组成,某同学用20克样品加入足量的稀硫酸中,待反应完全后过滤,称得不溶物质量为6克.试计算:(1)金属混合物中铁的质量分数.
(2)产生氢气的质量.
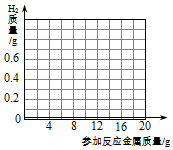
(3)在如图中画出产生氢气质量与参加反应的金属关系图象.
分析 由于铜排在了氢的后面所以不与酸反应,只有铁与硫酸反应,稀硫酸是足量的,所以不溶物为铜的质量,则铁的质量为20g-6g=14g,根据方程式列比例式进行计算,已知量是铁,即可求出氢气的质量.
解答 解:(1)由题意可知,铁的质量为:20g-6g=14g;
金属混合物中铁的质量分数为$\frac{14g}{20g}$×100%=70%.
(2)设生成氢气的质量为x.
Fe+H2SO4═FeSO4+H2↑
56 2
14g x
则 $\frac{56}{2}=\frac{14g}{x}$,解得x=0.5g.
答:产生氢气的质量是0.5g.
(3)根据计算结果,氢气质量与参加反应的金属关系图象为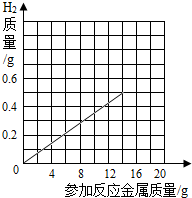
故答案为:(1)70%;(2)0.5g;(3)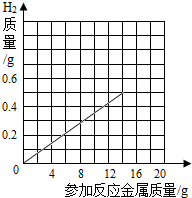
点评 解答本题的关键是要知道铜与硫酸不反应,因为铜排在了氢的后面,只有排在氢前面的金属才能与酸反应产生氢气.

练习册系列答案
 第1卷单元月考期中期末系列答案
第1卷单元月考期中期末系列答案
相关题目
15.小明打扫卫生时发现地砖上的铁锈(主要成分Fe203)用水很难清洗,决定运用所学知识解决这难题,他进行了如下活动:
①通过测试pH,寻找除锈剂,结果如表:
②将少量洁厕灵倒在地砖的锈斑上,进行擦拭冲洗,铁锈很快被清除;
③查阅资料得知,“洁厕灵”主要成分是一些酸和多种其它物质组成的混合物.
根据上述材料,请回答:
(1)上述物品中,酸性最强的是洁厕灵;
(2)如果洁厕灵中某酸的化学式为HR,该酸与铁锈反应的化学方程式:6HR+Fe2O3═2FeR3+3H2O.
①通过测试pH,寻找除锈剂,结果如表:
| 物品 | 食用醋 | 洗洁精 | 油污净 | 洁厕灵 |
| pH | 3 | 10 | 13 | 1 |
③查阅资料得知,“洁厕灵”主要成分是一些酸和多种其它物质组成的混合物.
根据上述材料,请回答:
(1)上述物品中,酸性最强的是洁厕灵;
(2)如果洁厕灵中某酸的化学式为HR,该酸与铁锈反应的化学方程式:6HR+Fe2O3═2FeR3+3H2O.
13.下列不属于合成材料的是( )
| A. | 玻璃钢 | B. | 有机玻璃 | C. | 涤纶 | D. | 合成橡胶 |
10.下列各组转化中,一定条件下不能一步实现的是( )
| A. | Na2CO3→Na2SO4 | B. | NH4NO3→NH3 | C. | Fe2O3→FeCl2 | D. | NaOH→Cu(OH)2 |
14.下列叙述中,错误的是( )
| A. | 溶质可以是固体、液体、气体 | |
| B. | 溶液都是均-、稳定的混合物 | |
| C. | 同种溶质的饱和溶液,一定比它的不饱和溶液的浓度大 | |
| D. | 析出晶体后的溶液一定是该温度下的饱和溶液 |
15.我校化学兴趣小组欲将粗盐提纯,再用制取的精盐配制7.5%的氯化钠溶液100g.下列说法不正确的是( )
| A. | 配制溶液时要称量7.5g氯化钠,量取92.5mL的水 | |
| B. | 本实验多次使用玻璃棒,有三种作用:搅拌、引流、转移 | |
| C. | 本实验提纯的氯化钠可能不纯,导致配制的氯化钠溶液质量分数偏大 | |
| D. | 本实验的主要步骤是溶解、过滤、蒸发和计算、称取、量取、溶解、转移 |