题目内容
5.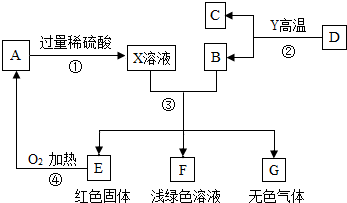 A、B、C、D、E、F、G为初中化学常见的物质,其中B、E、G属于单质,反应②是以赤铁矿为原料炼铁工业中的主要反应,它们之间的相互转化关系如图所示:
A、B、C、D、E、F、G为初中化学常见的物质,其中B、E、G属于单质,反应②是以赤铁矿为原料炼铁工业中的主要反应,它们之间的相互转化关系如图所示:(1)物质A的化学式是CuO;反应①的基本反应类型复分解反应;反应④的现象为红色固体变成黑色.
(2)写出反应②的化学方程式:3CO+Fe2O3$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2.
(3)写出反应③中生成无色气体G的化学方程式:Fe+H2SO4═FeSO4+H2↑.
分析 根据反应②是炼铁工业中的主要反应,B属于单质,所以B是铁,依据工业炼铁的原理可知,一般是一氧化碳和氧化铁反应生成铁和二氧化碳的反应,所以C是二氧化碳,A和过量的硫酸反应生成X溶液,X中应该有未反应完的硫酸,X和铁反应会生成红色固体单质E、浅绿色的溶液F、以及无色气体单质G,所以E是铜,F是硫酸亚铁,G是氢气,E和氧气反应生成A,所以A是氧化铜,将推出的各种物质代入转化关系中验证即可.
解答 解:根据反应②是炼铁工业中的主要反应,B属于单质,所以B是铁,依据工业炼铁的原理可知,一般是一氧化碳和氧化铁反应生成铁和二氧化碳的反应,所以C是二氧化碳,A和过量的硫酸反应生成X溶液,X中应该有未反应完的硫酸,X和铁反应会生成红色固体单质E、浅绿色的溶液F、以及无色气体单质G,所以E是铜,F是硫酸亚铁,G是氢气,E和氧气反应生成A,所以A是氧化铜,经过验证,推导正确,
(1)根据分析,A是CuO;反应①为氧化铜与稀硫酸反应生成硫酸铜和水,其基本反应类型复分解反应;反应④为铜与氧气反应生成氧化铜,其反应的现象为红色固体变成黑色.
(2)反应②是一氧化碳和氧化铁在高温的条件下反应生成铁和二氧化碳,化学方程式为:3CO+Fe2O3$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2;
(3)反应③中生成红色固体E的反应是铁和硫酸铜反应生成硫酸亚铁和铜,化学方程式为:Fe+CuSO4═Cu+FeSO4.
反应③中生成无色气体G的反应是铁与稀硫酸溶液反应生成硫酸亚铁和氢气,化学方程式为:Fe+H2SO4═FeSO4+H2↑.
故答案为:
(1)CuO;复分解反应; 红色固体变成黑色;
(2)3CO+Fe2O3$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2;(3)Fe+H2SO4═FeSO4+H2↑.
点评 在解此类题时,首先将题中有特征的物质推出,然后结合推出的物质和题中的转化关系推导剩余的物质,最后将推出的各种物质代入转化关系中进行验证即可.

 阅读快车系列答案
阅读快车系列答案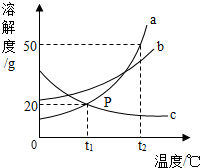 如图是a、b、c三种物质的溶解度曲线.下列叙述错误的是( )
如图是a、b、c三种物质的溶解度曲线.下列叙述错误的是( )| A. | t1℃时,a、c的溶解度相等 | |
| B. | t1℃时,a物质饱和溶液中溶质、溶剂的质量比为1:5 | |
| C. | t2℃时a、b、c的饱和溶液降温到0℃后,C液的溶质质量分数最大 | |
| D. | t2℃时30 g a物质的饱和溶液稀释成20%溶液需加入水的质量为20 g |
| A. | 铁丝伸入氧气中火星四射,生成黑色固体 | |
| B. | 在氢氧化钾溶液中滴加少量硫酸铜溶液,产生蓝色沉淀 | |
| C. | 部分变质的氢氧化钠溶液中滴加几滴稀盐酸,产生大量气泡 | |
| D. | 氯化铵与氢氧化钠溶液混合共热,产生的气体能使湿润的蓝色石蕊试纸变红 |
| A. | O3属于单质 | B. | SO2、NO2和CO都属于氧化物 | ||
| C. | SO2、NO2中都含有氧分子 | D. | 四种物质中都含有氧元素 |
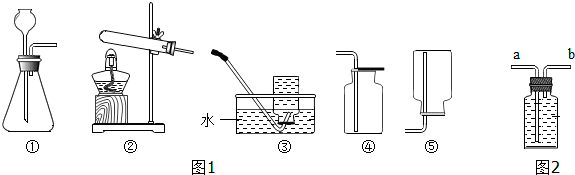
| A. | ②③④⑤① | B. | ④③②①⑤ | C. | ④②③①⑤ | D. | ②④③⑤① |
 标志的垃圾桶
标志的垃圾桶