题目内容
17. 黄铜是一种常见的合金材料,其主要成分为Cu、Zn,还含有少量不与酸反应的成分,现向一定质量的黄铜中加入体积为100mL,密度ρ=1.2g/mL的稀硫酸,产生H2的质量和硫酸溶液体积的关系如图所示,充分反应后溶液中剩余固体的质量为27g.
黄铜是一种常见的合金材料,其主要成分为Cu、Zn,还含有少量不与酸反应的成分,现向一定质量的黄铜中加入体积为100mL,密度ρ=1.2g/mL的稀硫酸,产生H2的质量和硫酸溶液体积的关系如图所示,充分反应后溶液中剩余固体的质量为27g.(1)观察图象,黄铜与硫酸充分反应后,硫酸是否有剩余?是(选填“是”或“否”)
(2)黄铜中Zn的质量分数为多少?(请列式计算,结果精确到0.1g)
分析 (1)根据图象中的数据可以看出,加入稀硫酸生成氢气0.4克后,随着硫酸体积的增加,气体不再增加进行分析;
(2)根据锌和硫酸反应生成硫酸锌和氢气,结合生成的氢气质量计算出锌的质量;
解答 解:(1)通过图象中的数据可以看出,加入稀硫酸生成氢气0.4克后,随着硫酸体积的增加,气体不再增加,所以硫酸有剩余;
(2)设样品中锌的质量为x
Zn+H2SO4═ZnSO4+H2↑
65 2
x 0.4g
$\frac{65}{x}=\frac{2}{0.4g}$
x=13g
所以黄铜中Zn的质量分数为$\frac{13g}{13g+27g}$×100%=32.5%;
故答案为:(1)是;(2)32.5%;
点评 本题主要考查有关化学方程式的计算和质量分数的计算,难度较大.

练习册系列答案
 口算能手系列答案
口算能手系列答案
相关题目
8.下列实验操作中正确的是( )
| A. |  滴加液体 | B. |  塞紧橡皮塞 | ||
| C. |  给液体加热 | D. |  检查装置的气密性 |
5.下列资源的利用过程中发生了化学变化的是( )
| A. | 海水晒盐 | B. | 干冰制冷 | C. | 风力发电 | D. | 铁矿炼铁 |
12.下列说法中正确的是( )
| A. | 用甲醛溶液浸泡海产品保鲜 | |
| B. | 微量元素是人体必需的营养素,多吃无害 | |
| C. | 向食品袋里冲入氦气延长食品的保质期 | |
| D. | 有机物是含碳的化合物,CO、CO2也是有机物 |
2. 某研究性学习小组在探究“锌与硫酸反应快慢的影响因素”时,发现一个意外现象:硫酸中混有硫酸铜溶液时,产生氢气的速率更快.
某研究性学习小组在探究“锌与硫酸反应快慢的影响因素”时,发现一个意外现象:硫酸中混有硫酸铜溶液时,产生氢气的速率更快.
【提出问题】是什么离子导致产生氢气的速率加快?
【猜想假设】甲同学:可能与铜离子有关;
乙同学:可能与硫酸根离子有关;…
丙同学认为乙的猜想不科学,理由是.
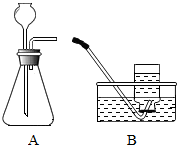
【实验验证】用A、B两组仪器进行实验:
步骤一:检查装置气密性.连接AB,用拇指堵住导管口,从长颈漏斗加水至一定高度,静置,观察液面不下降,即为气密性良好.
步骤二:量取2份质量分数为20%的稀硫酸各20mL,第一份加入质量分数为10%的硫酸铜溶液1mL,第二份加入质量分数为10%的硫酸锌溶液1mL.称取2份形状相同锌粒各1g,分别与以上溶液反应.反应装置如图A所示.用此装置实验时,长颈漏斗下端要插入液面以下,目的是.
步骤三:用B收集气体,分别记录收集一瓶气体(集气瓶规格均为125mL)所需的时间(如下表),什么时间开始收集气体?.
锌与硫酸反应的化学方程式是Zn+H2SO4=ZnSO4+H2↑.
【得出结论】硫酸中混有硫酸铜溶液时,产生氢气的速率加快与铜离子有关.实验②中加入质量分数为10%的硫酸锌溶液1mL的作用是加入的硫酸铜溶液对硫酸浓度会产生影响,加入等量的硫酸锌溶液是为了控制硫酸浓度变化对实验数据产生干扰.
【反思质疑】丁同学认为:锌与混有硫酸铜的硫酸溶液反应时,产生氢气的速率较快可能与铜单质有关,他质疑的理由是.
【继续探究】请你设计一个实验方案验证丁同学的观点是否正确.
 某研究性学习小组在探究“锌与硫酸反应快慢的影响因素”时,发现一个意外现象:硫酸中混有硫酸铜溶液时,产生氢气的速率更快.
某研究性学习小组在探究“锌与硫酸反应快慢的影响因素”时,发现一个意外现象:硫酸中混有硫酸铜溶液时,产生氢气的速率更快.【提出问题】是什么离子导致产生氢气的速率加快?
【猜想假设】甲同学:可能与铜离子有关;
乙同学:可能与硫酸根离子有关;…
丙同学认为乙的猜想不科学,理由是.
【实验验证】用A、B两组仪器进行实验:
步骤一:检查装置气密性.连接AB,用拇指堵住导管口,从长颈漏斗加水至一定高度,静置,观察液面不下降,即为气密性良好.
步骤二:量取2份质量分数为20%的稀硫酸各20mL,第一份加入质量分数为10%的硫酸铜溶液1mL,第二份加入质量分数为10%的硫酸锌溶液1mL.称取2份形状相同锌粒各1g,分别与以上溶液反应.反应装置如图A所示.用此装置实验时,长颈漏斗下端要插入液面以下,目的是.
步骤三:用B收集气体,分别记录收集一瓶气体(集气瓶规格均为125mL)所需的时间(如下表),什么时间开始收集气体?.
| 编号 | 20%的稀硫酸各20mL | 锌粒 | 收集1瓶氢气所需的时间 |
| ① | 加入质量分数为10%的硫酸铜溶液1mL | 1g | 2分10秒 |
| ② | 加入质量分数为10%的硫酸锌溶液1mL | 1g | 3分01秒 |
【得出结论】硫酸中混有硫酸铜溶液时,产生氢气的速率加快与铜离子有关.实验②中加入质量分数为10%的硫酸锌溶液1mL的作用是加入的硫酸铜溶液对硫酸浓度会产生影响,加入等量的硫酸锌溶液是为了控制硫酸浓度变化对实验数据产生干扰.
【反思质疑】丁同学认为:锌与混有硫酸铜的硫酸溶液反应时,产生氢气的速率较快可能与铜单质有关,他质疑的理由是.
【继续探究】请你设计一个实验方案验证丁同学的观点是否正确.
| 编号 | 实验步骤 | 实验现象比较 | 实验结论 |
| ① | 取1g锌粒于锥形瓶中, 加入20mL 20%的稀硫酸 | 产生氢气的速率较快与铜单质有关 | |
| ② |
9.我们掌握了有关酸碱盐的知识后,化学课上老师分别利用碳酸钠溶液,氢氧化钙溶液、稀盐酸、酚酞溶液中的两种混合给大家表演魔术,a、b、c、d是上述四种溶液中的一种,过程如表:
请你帮助同学们揭开魔术的秘密.
(1)a为酚酞溶液;
(2)请写出乙试管中发生反应的化学方程式Na2CO3+2HCl=2NaCl+H2O+CO2↑;
(3)将丙试管中的物质过滤,其滤液中溶质的组成可能有三种情况,请写出其中的一种情况NaOH、Ca(OH)2,为了验证你的猜想,你设计的方案是不用填.
(4)若将乙试管中的残液倒入甲试管中,可观察到红色溶液变为无色,且看到有气泡冒出,则该无色溶液中可能含有的离子是钠离子、氯离子.
| 操作步骤 | 1.取三支试管,分别加入a、b、c三种溶液 2.用胶头滴管往三支试管中分别滴加d溶液 | ||
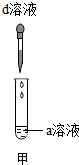 | 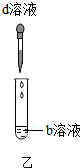 | 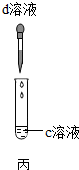 | |
| 魔术名称 | 变红酒 | 变汽水 | 变牛奶 |
| 现象 | 溶液呈红色 | 产生大量气泡 | 出现白色沉淀 |
(1)a为酚酞溶液;
(2)请写出乙试管中发生反应的化学方程式Na2CO3+2HCl=2NaCl+H2O+CO2↑;
(3)将丙试管中的物质过滤,其滤液中溶质的组成可能有三种情况,请写出其中的一种情况NaOH、Ca(OH)2,为了验证你的猜想,你设计的方案是不用填.
| 实验步骤 | 实验现象 | 结论 |
| 取少量滤液与试管中,加入碳酸钠溶液 | 有白色沉淀生成 | 猜想正确 |
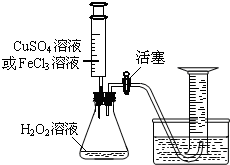 为比较相同浓度的FeCl3溶液和CuSO4溶液对H2O2分解的催化效果,某研究小组进行了如下探究:
为比较相同浓度的FeCl3溶液和CuSO4溶液对H2O2分解的催化效果,某研究小组进行了如下探究: