题目内容
氯化钠是生活必需品,也是重要的化工原料。提纯含少量泥沙的粗盐,一般要经过以下操作流程:
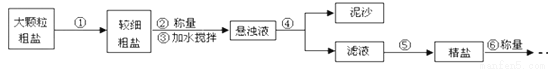
(1)操作①中必须用到的一种仪器是_______(填字母序号)。
A.研钵 B.量筒 C.烧杯 D.试管
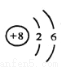
(2)操作④中需要将圆形滤纸折叠处理,下列图示中不该出现的情形是_____(填字母序号)。
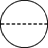 ,A)
,A)  ,B)
,B) 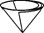 ,C)
,C) 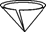 ,D)
,D)
(3)操作⑤中除用到三脚架、酒精灯、玻璃棒、坩埚钳外,还需要用到_________等仪器。该操作中容易造成食盐固体飞溅,为尽量减少飞溅,除连续搅拌外还可采取________________等措施。
(4) 若粗盐的质量为10g,室温时氯化钠溶解度为36.0 g,则操作③加入水的合适的量约为____(选填“15”、“30”或“60”)mL,选择的依据是_____ 。
A.节省实验时间 B.粗盐中的氯化钠能否完全溶解
C.烧杯、量筒的大小 D.由少到多,不够再加
A D 蒸发皿 间歇加热 30 AB 【解析】(1)大颗粒变成小颗粒需进行研磨;(2)根据图示中的滤纸的折叠处理进行分析;(3)根据粗盐提纯的步骤可知,⑤是蒸发,分析蒸发所用的仪器,并依据蒸发过程中的注意事项分析解答;(4)根据溶解度相关数据解答。(1)量筒是用来量取液体的体积的,烧杯是用来做大量液体的反应容器的,试管可以加热少量的液体,这三种仪器都是玻璃仪器,用力撞击会损坏,要将大颗粒... 手拉手全优练考卷系列答案
手拉手全优练考卷系列答案为了达到实验目的,下列实验方案或结论不正确的是( )
选项 | 实验目的 | 实验方案或结论 |
A | 除去氯化钾中的碳酸钾 | 取样、溶解、加入足量稀盐酸、蒸发 |
B | 除去炭粉中少量的氧化铜 | 将混合固体加入足量的稀盐酸中,充分反应后过滤、 洗涤、干燥 |
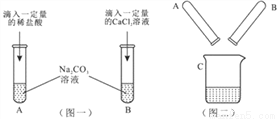
C | 鉴别四种溶液 ①CaCl2②Na2CO3③HCl④NaCl | 不用其他试剂就可以鉴别出来 |
D | 鉴定某溶液中是否含有硫酸根离子 | 取少量溶液于试管中,滴加BaCl2溶液和稀硝酸,出现白色沉淀不消失,则该溶液中一定有硫酸根离子 |
A. A B. B C. C D. D
D 【解析】 选项 实验目的 实验方案或结论 A 除去氯化钾中的碳酸钾 取样、溶解、加入足量稀盐酸、与碳酸钾反应生成氯化钾,水和二氧化碳,蒸发,故A正确; B 除去炭粉中少量的氧化铜 将混合固体加入足量的稀盐酸中,与氧化铜反应生成氯化铜和水,炭粉不溶于水,充分反应后过滤、洗涤、干燥,故B正确; C 鉴别四种溶液 ①CaC...下表中,除去物质所含少量杂质的方法正确的是( )
选项 | 物质 | 所含杂质 | 除去杂质的方法 |
A | KCl | KClO3 | 加少量 MnO2 加热 |
B | NaOH 溶液 | Ba(OH)2 | 先加入 CuSO4 溶液,再过滤 |
C | CuSO4 溶液 | FeSO4 | 加足量铜粉,过滤 |
D | CaCl2 溶液 | HCl | 加过量 CaCO3 粉末,过滤 |
A. A B. B C. C D. D
D 【解析】 选项 物质 所含杂质 除去杂质的方法 A KCl KClO3 加少量MnO2,促使KClO3分解生成氯化钾,二氧化锰不溶于水,加热,溶解,过量,结晶,故A错误; B NaOH 溶液 Ba(OH)2 先加入 CuSO4 溶液,与氢氧化钡反应生成硫酸钡白色沉淀和...

 ⑤
⑤
 B.
B.  C.
C.  D.
D. 
